Hvor mange gram HCI kan fremstilles fra 2,00 mol H2SO4 og 150 g NaCl?
1. Afbalanceret kemisk ligning
Reaktionen mellem svovlsyre (H₂so₄) og natriumchlorid (NaCI) producerer saltsyre (HCI) og natriumsulfat (Na₂so₄):
H₂so₄ + 2naCl → 2HCl + Na₂so₄
2. Bestem den begrænsende reaktant
* h₂so₄: Du har 2,00 mol H₂so₄.
* NaCl: Konverter gram NaCl til moller ved hjælp af dens molære masse (58,44 g/mol):
150 g NaCl * (1 mol NaCl / 58,44 g NaCl) =2,57 mol NaCl
For at finde den begrænsende reaktant skal du sammenligne molforholdet mellem reaktanter og den afbalancerede ligning:
* h₂so₄: 2,00 mol H₂so₄ / 1 =2,00
* NaCl: 2,57 mol NaCl / 2 =1,29
Den mindre værdi (1,29) svarer til NaCl. Dette betyder, at NaCl er den begrænsende reaktant, fordi det vil blive fuldstændigt konsumeret, før alle H₂so₄ er brugt op.
3. Beregn molen af produceret HCL
Ved hjælp af støkiometrien fra den afbalancerede ligning kan vi finde molen af HCL produceret:
2,57 mol NaCl * (2 mol HCI / 2 mol NaCl) =2,57 mol HCI
4. Konverter mol HCL til gram
Brug den molære masse af HCI (36,46 g/mol) til at konvertere mol til gram:
2,57 mol HCI * (36,46 g HCI / 1 mol HCI) = 93,7 g HCl
Derfor kan 93,7 gram HCL fremstilles ud fra de givne mængder af reaktanter.
Sidste artikelHvilken har mere masse en mol kalium eller natrium?
Næste artikelHvor mange mol (NH4) 2s er der i 150 g (NH4) 2s?
 Varme artikler
Varme artikler
-
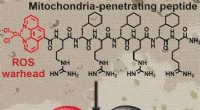 Et metallopeptid målretter og forstyrrer mitokondrielfunktionen i brystkræftstamcellerKredit:Wiley At dræbe maligne mitokondrier er en af de mest lovende fremgangsmåder i udviklingen af nye lægemidler mod kræft. Forskere fra Storbritannien har nu syntetiseret et kobberholdigt p
Et metallopeptid målretter og forstyrrer mitokondrielfunktionen i brystkræftstamcellerKredit:Wiley At dræbe maligne mitokondrier er en af de mest lovende fremgangsmåder i udviklingen af nye lægemidler mod kræft. Forskere fra Storbritannien har nu syntetiseret et kobberholdigt p -
 Ny teknologi fuldender vital klasse af industrielle reaktioner fem gange hurtigereNUS-forskerteamet ledet af Assoc Prof Yan Ning (midten) brugte en elektrostationsmaskine til at opnå den ønskede oscillation af elektriske potentialer for at fremskynde hydrogeneringen i en reaktor i
Ny teknologi fuldender vital klasse af industrielle reaktioner fem gange hurtigereNUS-forskerteamet ledet af Assoc Prof Yan Ning (midten) brugte en elektrostationsmaskine til at opnå den ønskede oscillation af elektriske potentialer for at fremskynde hydrogeneringen i en reaktor i -
 Flyveaske geopolymerbeton:Betydeligt forbedret modstandsdygtighed over for ekstremt alkaliangrebGeopolymer betonblokke, varmehærdet ved 200 grader Celsius og derefter nedsænket i et ekstremt alkalisk medium i 14 dage ved 80 grader Celsius (a og b), modstå angrebet væsentligt bedre end blokke var
Flyveaske geopolymerbeton:Betydeligt forbedret modstandsdygtighed over for ekstremt alkaliangrebGeopolymer betonblokke, varmehærdet ved 200 grader Celsius og derefter nedsænket i et ekstremt alkalisk medium i 14 dage ved 80 grader Celsius (a og b), modstå angrebet væsentligt bedre end blokke var -
 Skræddersyning af overfladen af kulstof kan indeholde nøglen til overvågning af patientblod i r…Det uendelige antal lokale atomstrukturer dannet af kulstof kan grupperes i et par motiver med karakteristiske atomare og elektroniske egenskaber. Kredit:Aalto University De potentielle anvendelse
Skræddersyning af overfladen af kulstof kan indeholde nøglen til overvågning af patientblod i r…Det uendelige antal lokale atomstrukturer dannet af kulstof kan grupperes i et par motiver med karakteristiske atomare og elektroniske egenskaber. Kredit:Aalto University De potentielle anvendelse
- Hvad er den mest magtfulde årsag til erosion?
- Hvad var rumfartøjet, som astronauter tog fra Apollo 11 til måneoverfladen kaldet?
- Hvordan ændrer geosfæren sig?
- Hvor ligger jorden ved Mælkevejen?
- Hvordan er en amfibier internt skelet for dens overlevelse?
- Xerox afslutter fusionen med Fujifilm til sejr for aktionærerne


