Hvad er den afbalancerede halvt ligning for brom og kaliumiodid?
reaktionen:
Brom (Br₂) reagerer med kaliumiodid (Ki) for at danne jod (I₂) og kaliumbromid (KBR).
Den afbalancerede samlede ligning:
Br₂ (l) + 2ki (aq) → 2kbr (aq) + i₂ (s)
Half-Ægning:
1. Oxidation halvt ligning:
* Iodidioner (I⁻) oxideres til jod (i₂).
* 2i⁻ (aq) → i₂ (s) + 2e⁻
2. Reduktion Half-ligning:
* Brommolekyler (BR₂) reduceres til bromidioner (BR⁻).
* br₂ (l) + 2e⁻ → 2BR⁻ (aq)
Forklaring:
* Oxidation: Iodidionerne (i⁻) mister elektroner, og deres oxidationstilstand stiger fra -1 til 0.
* reduktion: Brommolekylerne (BR₂) får elektroner, og deres oxidationstilstand falder fra 0 til -1.
Vigtige noter:
* Antallet af elektroner, der er mistet i oxidationens halvt ligning, skal svare til antallet af elektroner, der er opnået i reduktionen halvt ligning.
* Derfor multiplicerede vi reduktionen halvt ligning med 2.
* Disse halvt ligninger kan kombineres for at få den samlede afbalancerede ligning.
 Varme artikler
Varme artikler
-
 Forskere afslører mekanisme for dioxygenaktiveringKredit:Pixabay/CC0 Public Domain Metalloenzym kan koble dioxygenaktivering til substratfunktionalisering, som ofte udviser uovertruffen effektivitet, selv under omgivende forhold. Det menes, at m
Forskere afslører mekanisme for dioxygenaktiveringKredit:Pixabay/CC0 Public Domain Metalloenzym kan koble dioxygenaktivering til substratfunktionalisering, som ofte udviser uovertruffen effektivitet, selv under omgivende forhold. Det menes, at m -
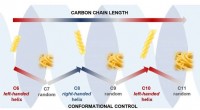 Kulstofkæder antager fusilli- eller spaghetti-former, hvis de har ulige eller lige talBilledet viser, hvordan konformationen (formen) af vores carbonkæder veksler mellem ordnede og kaotiske strukturer, da carbonkæden veksler mellem at have lige og ulige antal atomer. Kredit:University
Kulstofkæder antager fusilli- eller spaghetti-former, hvis de har ulige eller lige talBilledet viser, hvordan konformationen (formen) af vores carbonkæder veksler mellem ordnede og kaotiske strukturer, da carbonkæden veksler mellem at have lige og ulige antal atomer. Kredit:University -
 Formændrende element har nøglen til antibakteriel belægningAfbildet fra venstre til højre:University of Canterbury ph.d.-studerende Rukmini Gorthy og Johann Land og forskningsleder Maskin- og materialteknik Professor Susan Krumdieck er medforfattere på et pap
Formændrende element har nøglen til antibakteriel belægningAfbildet fra venstre til højre:University of Canterbury ph.d.-studerende Rukmini Gorthy og Johann Land og forskningsleder Maskin- og materialteknik Professor Susan Krumdieck er medforfattere på et pap -
 Bio-inspireret hydrogel kan hurtigt skifte til stiv plastGelen er blød og gennemsigtig ved 25°C og kan ikke bære en vægt på 10 kg (toppaneler), men den bliver hurtigt stiv og uigennemsigtig, når den opvarmes til 60°C, bliver stærk nok til at bære vægten (bu
Bio-inspireret hydrogel kan hurtigt skifte til stiv plastGelen er blød og gennemsigtig ved 25°C og kan ikke bære en vægt på 10 kg (toppaneler), men den bliver hurtigt stiv og uigennemsigtig, når den opvarmes til 60°C, bliver stærk nok til at bære vægten (bu


