Forskere afslører mekanisme for dioxygenaktivering
Kredit:Pixabay/CC0 Public Domain
Metalloenzym kan koble dioxygenaktivering til substratfunktionalisering, som ofte udviser uovertruffen effektivitet, selv under omgivende forhold.
Det menes, at metal-superoxo-mellemprodukter dannes ved dioxygenaktivering, og derefter yderligere reduceret til metal-peroxo og i sidste ende til -oxo-arter. Imidlertid, kemien af metal-superoxo-komplekser forbliver stort set ukendt.
I deres tidligere undersøgelse, forskere ledet af prof. Ye Shengfa fra Dalian Institute of Chemical Physics (DICP) ved det kinesiske videnskabsakademi og deres samarbejdspartnere opdagede, at behandling af divalent Mn(II), Fe(II), og Co(II)-modelkomplekser og/eller enzymer med dioxygen-genererede tilsvarende kortlivede trivalente metal-superoxo-mellemprodukter. De kunne omdannes til trivalente metal-hydroperoxo-arter via H-atomabstraktion.
For nylig, forskerne undersøgte reaktionerne af et Mn(III)-superoxo-kompleks med Brønsted- og Lewis-syrer ved hjælp af resonans-Raman, multi-frekvens elektron paramagnetiske resonansspektroskopier kombineret med kvantekemiske beregninger.
De afslørede, at Mn(III)-superoxo-komplekset undergik proton- og metalkoblet elektronoverførsel for at give en Mn(IV)-hydroperoxo- og en Mn(IV)-peroxo-Sc(III)-art, henholdsvis, derved manifesterer ambifil karakter af metal-superoxo-komplekser.
Denne hidtil usete metode til at generere superoxo-til-peroxo-konvertering repræsenterer et vigtigt skridt mod bedre forståelse af dioxygenaktivering og evolutionsprocesser, der forekommer i metalloenzymer og kunstige katalysatorer.
Undersøgelsen blev offentliggjort i Journal of the American Chemical Society .
 Varme artikler
Varme artikler
-
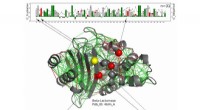 Arbejdsproteiner gør god brug af frustrationI denne strukturelle model for et beta-lactamase-protein, Katalytiske rester er vist som kugler med dem, der konsekvent er stærkt frustrerede langs hele beta-lactamase-familien vist med rødt, og dem,
Arbejdsproteiner gør god brug af frustrationI denne strukturelle model for et beta-lactamase-protein, Katalytiske rester er vist som kugler med dem, der konsekvent er stærkt frustrerede langs hele beta-lactamase-familien vist med rødt, og dem, -
 Skorpiongift til at transportere stoffer ind i hjernenKæmpe gul israelsk skorpion. Kredit:Ester Inbar Peptider- og proteinlaboratoriet ved Institut for Forskning i Biomedicin (IRB Barcelona) har udgivet en artikel i Kemisk kommunikation beskriver b
Skorpiongift til at transportere stoffer ind i hjernenKæmpe gul israelsk skorpion. Kredit:Ester Inbar Peptider- og proteinlaboratoriet ved Institut for Forskning i Biomedicin (IRB Barcelona) har udgivet en artikel i Kemisk kommunikation beskriver b -
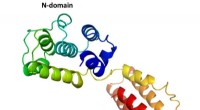 Forskere spoler i strukturen af laksevirusDen første komplette struktur af et M1-protein fra en infektiøs lakseanæmivirus, som afsløret af forskere ved Rice University. Strukturen af proteinet, som danner et beskyttende skjold omkring det v
Forskere spoler i strukturen af laksevirusDen første komplette struktur af et M1-protein fra en infektiøs lakseanæmivirus, som afsløret af forskere ved Rice University. Strukturen af proteinet, som danner et beskyttende skjold omkring det v -
 Materiale til sikrere fodboldhjelme kan reducere hovedskaderHRL Laboratories Microlattice Impact Attenuator Pads er lavet med Light-Casting Technology, der gør hjelme bedre til at beskytte bæreren og meget nemmere at have på hovedet på grund af den øgede lufts
Materiale til sikrere fodboldhjelme kan reducere hovedskaderHRL Laboratories Microlattice Impact Attenuator Pads er lavet med Light-Casting Technology, der gør hjelme bedre til at beskytte bæreren og meget nemmere at have på hovedet på grund af den øgede lufts
- Naturlige enzymer filtrerer hormonforstyrrende kemikalier fra spildevand
- Filippinske slanger arter
- Mysteriesignal fra rummet er løst. Det er ikke aliens
- Videnskab følger af lodne mysterier
- Deepwater Horizon Oil fundet i landbaserede fugle for første gang
- Forskellen mellem afhjælpning og intervention i matematik


