Hvis et bromatom tiltrækker elektron fra kalium, hvad sker der med begge dele?
* ionisk bindingsdannelse: Brom (BR) er en ikke -metal med en høj elektronegativitet (tendens til at tiltrække elektroner), mens kalium (K) er et metal med lav elektronegativitet. Når de reagerer, tiltrækker brom kraftigt en elektron fra kalium. Denne overførsel af en elektron resulterer i dannelsen af en ionisk binding.
* iondannelse:
* kalium (k) Mister en elektron og bliver en positivt ladet ion kaldet en kaliumkation (K+).
* brom (Br) Får en elektron og bliver en negativt ladet ion kaldet en bromidanion (BR-).
* Elektrostatisk attraktion: De modsatte ladede ioner (K+ og Br-) tiltrækkes nu af hinanden på grund af elektrostatiske kræfter. Denne attraktion holder dem sammen i en ionisk forbindelse.
* Dannelse af kaliumbromid (KBR): Den resulterende ioniske forbindelse er kaliumbromid (KBR). Det er et hvidt krystallinsk fast stof, der ofte bruges i medicin og fotografering.
Kortfattet:
Bromatomet tiltrækker et elektron fra kaliumatomet og danner en kaliumkation (K+) og en bromidanion (BR-). Disse ioner holdes derefter sammen af elektrostatiske kræfter, hvilket resulterer i dannelsen af den ioniske sammensatte kaliumbromid (KBR).
 Varme artikler
Varme artikler
-
 Unik ferroelektrisk mikrostruktur afsløret for første gangEt atomisk opløst scanningstransmissionselektronmikroskopi (STEM) billede af de polære nanoregioner (PNRer) indlejret i den ikke-polære matrix i det lagdelte perovskitmateriale (Ca, Sr)3Mn2O7. Lys kon
Unik ferroelektrisk mikrostruktur afsløret for første gangEt atomisk opløst scanningstransmissionselektronmikroskopi (STEM) billede af de polære nanoregioner (PNRer) indlejret i den ikke-polære matrix i det lagdelte perovskitmateriale (Ca, Sr)3Mn2O7. Lys kon -
 Nobel Kemipris:Stor pris for molekylære forholdKredit:Wikipedia Nobelprisen i kemi belønner forskere for store fremskridt i at studere de uendeligt små stykker materiale, der er livets byggesten. De seneste priser er gået til forskere, der ud
Nobel Kemipris:Stor pris for molekylære forholdKredit:Wikipedia Nobelprisen i kemi belønner forskere for store fremskridt i at studere de uendeligt små stykker materiale, der er livets byggesten. De seneste priser er gået til forskere, der ud -
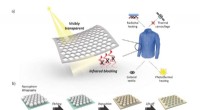 Ny nanofotonisk belægning kunne hjælpe med termisk styring og modovervågninga) Skematisk af VTIR for at blokere emissionen af termisk stråling til strålingsopvarmning og termisk camouflage. b) Skematisk fremstilling af fremstillingsprocessen og SEM-billeder for VTIR-belægni
Ny nanofotonisk belægning kunne hjælpe med termisk styring og modovervågninga) Skematisk af VTIR for at blokere emissionen af termisk stråling til strålingsopvarmning og termisk camouflage. b) Skematisk fremstilling af fremstillingsprocessen og SEM-billeder for VTIR-belægni -
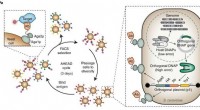 Nyt værktøj har til formål at bekæmpe COVID-19, andre sygdommeFig. 1:Autonom hypermutation gæroverfladevisning (AHEAD). en, Skema for den hurtige udvikling af højaffinitetsbinding ved hjælp af AHEAD. Ab, antistoffragment; DNAP, DNA-polymerase; HA, hæmagglutinin
Nyt værktøj har til formål at bekæmpe COVID-19, andre sygdommeFig. 1:Autonom hypermutation gæroverfladevisning (AHEAD). en, Skema for den hurtige udvikling af højaffinitetsbinding ved hjælp af AHEAD. Ab, antistoffragment; DNAP, DNA-polymerase; HA, hæmagglutinin
- Ekstrem drivhuseffekt opvarmede den unge jord
- Uligheden du ikke kan ændre, der varer livet ud
- Hvilken nitrogenholdig base er til stede i RNA, men ikke DNA?
- Hvad er åbningen på undersiden af et blad, der forhindrer vand i at fordampe?
- Mærkelige gadgets på CES:Motoriseret ethjulet cykel, nogen?
- Forskelle mellem ekstrusive og påtrængende klipper


