Hvad sker der, når natriumhydroxid tilsættes dråbevis til opløsning, der kontakter phenolphthalein?
1. Indledende tilstand:
* phenolphthalein -opløsning: Phenolphthalein er en farveløs indikator i sure eller neutrale opløsninger.
* natriumhydroxid (NaOH): En stærk base.
2. Tilføjelse af NaOH dråbevis:
* Når du tilføjer NaOH -dråber, bliver opløsningen mere grundlæggende (alkalisk).
* Nøglepunkt: Phenolphthalein ændrer farve i grundlæggende løsninger.
3. Farveændring:
* ved en bestemt pH: Når opløsningen når en lidt basisk pH (ca. 8,2 - 10), gennemgår phenolphthalein -molekylerne en strukturel ændring. Denne ændring får dem til at absorbere lys forskelligt, hvilket resulterer i en lyserød farve .
4. Reaktionen:
* NaOH adskiller sig i vand for at danne hydroxidioner (OH-):
NaOH (aq) → Na + (aq) + OH- (aq)
* Hydroxidionerne reagerer med phenolphthalein, hvilket forårsager farveændringen.
Kortfattet:
Tilsætning af natriumhydroxid dråbevis til en phenolphthalein -opløsning får opløsningen til at blive grundlæggende. Når pH når et lidt grundlæggende interval, skifter phenolphthalein farve fra farveløs til lyserød, hvilket indikerer tilstedeværelsen af en grundlæggende opløsning.
 Varme artikler
Varme artikler
-
 Lab træder på gassen for at forbedre kemisk produktionIn situ og ex situ røntgenfotoelektronspektroskopi og elektronmikroskopi afslører stabiliteten af nikkelkobberlegeringskatalysatorer til ikke-oxidativ ethanoldehydrogenering forbedres ved at generer
Lab træder på gassen for at forbedre kemisk produktionIn situ og ex situ røntgenfotoelektronspektroskopi og elektronmikroskopi afslører stabiliteten af nikkelkobberlegeringskatalysatorer til ikke-oxidativ ethanoldehydrogenering forbedres ved at generer -
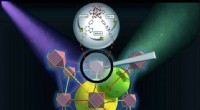 Brug porøse krystaller til at høste lysDen metalorganiske ramme (MOF) indeholder zirconiumbaserede knuder (lilla cuboctahedra) forbundet med kulstofbaserede linkermolekyler (røde og gule stænger) for at danne en porøs struktur med to store
Brug porøse krystaller til at høste lysDen metalorganiske ramme (MOF) indeholder zirconiumbaserede knuder (lilla cuboctahedra) forbundet med kulstofbaserede linkermolekyler (røde og gule stænger) for at danne en porøs struktur med to store -
 Bekæmpelse af et mægtigt ukrudtKredit:CC0 Public Domain Ukrudt er irriterende i enhver situation. Nu, forestil dig et ukrudt, der er så besværligt, at det har muteret til at modstå flere herbicider. Palmer amaranth, et medlem a
Bekæmpelse af et mægtigt ukrudtKredit:CC0 Public Domain Ukrudt er irriterende i enhver situation. Nu, forestil dig et ukrudt, der er så besværligt, at det har muteret til at modstå flere herbicider. Palmer amaranth, et medlem a -
 Bygger molekyler som Tinkertoys? Et banebrydende studie kan bane vejenEt team af kemikere ved University of Chicago annoncerede en ny teknik, der gør det muligt for forskere let at skære nitrogenatomer fra molekyler-hvilket kan gøre processen med at finde nye molekyler
Bygger molekyler som Tinkertoys? Et banebrydende studie kan bane vejenEt team af kemikere ved University of Chicago annoncerede en ny teknik, der gør det muligt for forskere let at skære nitrogenatomer fra molekyler-hvilket kan gøre processen med at finde nye molekyler


