Er metal mest sandsynligt at danne en ion ved at miste elektroner eller vinde?
* Metallisk natur: Metaller har relativt få elektroner i deres ydre skal (valenselektroner).
* Elektropositivitet: Metaller har en tendens til at have lave ioniseringsenergier, hvilket betyder, at det ikke kræver meget energi for at fjerne et elektron fra deres ydre skal.
* tendens til at danne kationer: Ved at miste elektroner opnår metaller en stabil elektronkonfiguration, der ofte ligner en ædel gas. Den resulterende positivt ladede ion kaldes en kation.
Eksempel: Natrium (NA) har en valenselektron. Den mister let denne elektron til dannelse af en natriumkation (Na+), som har den samme elektronkonfiguration som den ædle gas neon (NE).
Fortæl mig, hvis du har andre spørgsmål!
 Varme artikler
Varme artikler
-
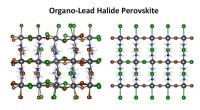 Forskere udvikler innovative teknikker til højopløsningsanalyse af hybridmaterialerSkematisk af organo-blyhalogenidperovskit, der viser forvrængninger fra tilfældige halogenidpositioner (venstre) versus ordnede halogenidpositioner (højre). Et Berkeley Lab-studie viser, at der findes
Forskere udvikler innovative teknikker til højopløsningsanalyse af hybridmaterialerSkematisk af organo-blyhalogenidperovskit, der viser forvrængninger fra tilfældige halogenidpositioner (venstre) versus ordnede halogenidpositioner (højre). Et Berkeley Lab-studie viser, at der findes -
 Enhedsopdatering muliggør mobiltest for vira, bakterier og aktive toksinerSandia National Laboratories kemiker Chung-Yan Koh, venstre, og tidligere Sandia bioingeniør Chris Phaneuf, ret, behold den nyligt opdaterede SpinDx diagnostiske enhed. Kredit:Jules Bernstein Du s
Enhedsopdatering muliggør mobiltest for vira, bakterier og aktive toksinerSandia National Laboratories kemiker Chung-Yan Koh, venstre, og tidligere Sandia bioingeniør Chris Phaneuf, ret, behold den nyligt opdaterede SpinDx diagnostiske enhed. Kredit:Jules Bernstein Du s -
 Nedbrydelige belægninger til komposterbar papiremballage til fødevarer blokerer fedt og olieKredit:Unsplash/CC0 Public Domain Kopper, kartoner og madindpakninger lavet af papir kan virke som om de ville være biologisk nedbrydelige, men mange indeholder en plastbelægning, der ikke kan kom
Nedbrydelige belægninger til komposterbar papiremballage til fødevarer blokerer fedt og olieKredit:Unsplash/CC0 Public Domain Kopper, kartoner og madindpakninger lavet af papir kan virke som om de ville være biologisk nedbrydelige, men mange indeholder en plastbelægning, der ikke kan kom -
 Computermodel til design af proteinsekvenser, der er optimeret til at binde til lægemiddelmålVed at bruge en computermodelleringstilgang, som de udviklede, MIT-biologer identificerede tre forskellige proteiner, der kan binde selektivt til hver af tre lignende mål, alle medlemmer af Bcl-2-fami
Computermodel til design af proteinsekvenser, der er optimeret til at binde til lægemiddelmålVed at bruge en computermodelleringstilgang, som de udviklede, MIT-biologer identificerede tre forskellige proteiner, der kan binde selektivt til hver af tre lignende mål, alle medlemmer af Bcl-2-fami
- Hvad er ordet ligning for jernuldforbrænding i rent ilt for at producere oxid?
- Hvordan man opbygger et DNA Molecule School Project
- En ernæringsmæssig kalorie er lig med 100 kalorier?
- Hvor mange 200 mcg -tabletter svarede til 20 mg tabletter?
- Hvad er arachnoider?
- Et myggenes hemmelige våben:en let berøring og stærke vinger


