Hvad ville have den laveste damptrykalkohol i vand eller sukkerbenzen NaCl Pure alle består af 1,00 m opløsning?
Forståelse af damptryk og kolligative egenskaber
* damptryk: Det tryk, der udøves af dampen af en væske i ligevægt med dens kondenserede fase.
* Kolligative egenskaber: Egenskaber ved løsninger, der kun afhænger af antallet af tilstedeværende opløste partikler, ikke deres identitet.
* damptryk sænkning: En af de kolligative egenskaber. Tilsætning af et ikke-flygtigt opløst stof til et opløsningsmiddel sænker opløsningsmidlets damptryk.
Faktorer, der påvirker damptryk sænkning
1. Ikke-flygtige opløste stoffer (dem, der ikke let fordamper) forårsager det største damptryksænkende.
2. Koncentration af opløsningen: Jo højere koncentration af opløste partikler er, jo større er nedsat damptryk.
analyse af løsningen
* alkohol i vand: Alkohol er noget flygtigt, så dens damptrykssænkning vil være mindre udtalt sammenlignet med et helt ikke-flygtigt opløst stof.
* sukker i benzen: Sukker er ikke-flygtig, og benzen er et flygtigt opløsningsmiddel. Denne kombination vil resultere i et betydeligt damptryksænkende.
* NaCl i vand: NaCl er ionisk og dissocieres i to partikler (Na+ og Cl-), når de opløstes i vand. Dette skaber en højere koncentration af opløste partikler, hvilket fører til en større sænkning af damptryk sammenlignet med et ikke-ionisk opløst stof ved den samme molaritet.
* ren: Et rent stof har intet opløst stof, så dets damptryk vil være det højeste.
Konklusion
Løsningen med laveste damptryk ville være NaCl i vand fordi:
1. NaCl er et ikke-flygtigt opløst stof.
2. NaCl dissocieres i to ioner pr. Formelenhed, hvilket øger antallet af opløste partikler.
Vigtig note: Opløsningerne er alle 1,00 m (molal), hvilket betyder, at de indeholder 1 mol opløst stof pr. Kg opløsningsmiddel. Dette giver os mulighed for at sammenligne de løsninger, der udelukkende er baseret på arten af opløsningen og dens tendens til at sænke damptrykket.
 Varme artikler
Varme artikler
-
 Farveændringstest for at hjælpe kræftforskningen videreKredit:shapecharge iStock En simpel farveændringstest til at hjælpe videnskabsmænd med at undersøge potentielle kræftlægemidler er blevet udviklet af University of Bath-forskere, gør det muligt fo
Farveændringstest for at hjælpe kræftforskningen videreKredit:shapecharge iStock En simpel farveændringstest til at hjælpe videnskabsmænd med at undersøge potentielle kræftlægemidler er blevet udviklet af University of Bath-forskere, gør det muligt fo -
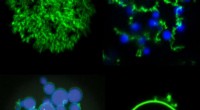 Varme og lys skaber nye biokompatible mikropartiklerBlandinger af POPer (grøn) og ELPer (blå) kan bruges til at skabe en række nye mikropartikelarkitekturer, herunder (med uret fra øverst til venstre) porøse partikler, frugt-på-vin-netværk, enkelte hul
Varme og lys skaber nye biokompatible mikropartiklerBlandinger af POPer (grøn) og ELPer (blå) kan bruges til at skabe en række nye mikropartikelarkitekturer, herunder (med uret fra øverst til venstre) porøse partikler, frugt-på-vin-netværk, enkelte hul -
 Kontaktsporingssystem for kemisk eksponering i miljøetEmory-forskere kunne identificere personer, der tog forskellige medikamenter, baseret på mønsteret af lægemiddelmetabolitter efterladt i kroppen. Medicinen omfattede acetaminophen, det antidepressive
Kontaktsporingssystem for kemisk eksponering i miljøetEmory-forskere kunne identificere personer, der tog forskellige medikamenter, baseret på mønsteret af lægemiddelmetabolitter efterladt i kroppen. Medicinen omfattede acetaminophen, det antidepressive -
 Gennembrud for retshåndhævelse til hurtigt at skelne mellem hamp og kontrolleret marihuanaHamp Synergistics, LLC, en bioteknologivirksomhed dedikeret til at transformere den måde, forbrugerne bruger hamp-afledte cannabinoid-baserede formuleringer, har dannet et partnerskab med førende rets
Gennembrud for retshåndhævelse til hurtigt at skelne mellem hamp og kontrolleret marihuanaHamp Synergistics, LLC, en bioteknologivirksomhed dedikeret til at transformere den måde, forbrugerne bruger hamp-afledte cannabinoid-baserede formuleringer, har dannet et partnerskab med førende rets
- Flowfysik kan hjælpe prognosemænd med at forudsige ekstreme begivenheder
- Tyfonen Souliks store øje på NASAs satellitbilleder
- Forskere lukker ind om kilden til shetlandske tsunamier
- Hvorfor ville forskere gerne oprette et hybrid menneske-ko-embryo?
- Multiple choice-eksamener favoriserer drenge frem for piger, forværring af den matematiske kønsfor…
- Ny laserkrystal fremstår som en lovende kandidat til 2,7 μm lasere


