Hvorfor er vand ikke blandbart med methylenchlorid?
* vand (H₂O) er et polært molekyle . Dette betyder, at det har en delvis positiv ladning på brintatomerne og en delvis negativ ladning på iltatomet på grund af den ujævne deling af elektroner. Denne polaritet giver vandmolekyler mulighed for at danne stærke brintbindinger med hinanden.
* methylenchlorid (ch₂cl₂) er et ikke-polært molekyle . Kulstof- og kloratomerne har lignende elektronegativitet, hvilket resulterer i en jævn fordeling af ladning. Dette betyder, at methylenchloridmolekyler ikke kan danne stærke hydrogenbindinger med vandmolekyler.
som opløser som: Polære opløsningsmidler som vand opløser polære opløste stoffer og ikke-polære opløsningsmidler som methylenchlorid opløser ikke-polære opløste stoffer. På grund af deres kontrasterende polariteter er vand og methylenchlorid ublandbart , hvilket betyder, at de ikke blander og danner separate lag, når de kombineres.
De stærkere intermolekylære kræfter mellem vandmolekyler (hydrogenbindinger) er meget stærkere end kræfterne mellem vand og methylenchloridmolekyler, hvilket forhindrer dem i at blande.
Sidste artikelHvor mange hydrogenatomer har kulstof?
Næste artikelHvorfor opløse BR2 i methylenchlorid og ikke vand?
 Varme artikler
Varme artikler
-
 Inspireret af knogler, nyt adaptivt materiale styrkes fra vibrationerPME-forskere har udviklet et nyt gelmateriale (hvidt), der efterligner knogler og bliver stærkere, når det udsættes for vibrationer, hvilket kunne føre til nye klæbemidler og bedre måder at integrere
Inspireret af knogler, nyt adaptivt materiale styrkes fra vibrationerPME-forskere har udviklet et nyt gelmateriale (hvidt), der efterligner knogler og bliver stærkere, når det udsættes for vibrationer, hvilket kunne føre til nye klæbemidler og bedre måder at integrere -
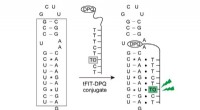 Ny måde at identificere influenza A-virus lyser op, når specifikke virusmål er til stedeSkematisk illustration af fluorescensføling af panhandle-strukturen af IAV RNA-promotorregionen (angivet i boksen). Kredit:tFIT-DPQ sonde. Influenza A-virus, som er ansvarlig for sæsonbestemte in
Ny måde at identificere influenza A-virus lyser op, når specifikke virusmål er til stedeSkematisk illustration af fluorescensføling af panhandle-strukturen af IAV RNA-promotorregionen (angivet i boksen). Kredit:tFIT-DPQ sonde. Influenza A-virus, som er ansvarlig for sæsonbestemte in -
 Sporing af atombevægelse i realtid mellem krystalkorn i metallerTing Zhu, professor i maskinteknik ved Georgia Tech, foran sine TEM-billeder af polykrystallinske metaller og en grafisk simulerende atomstruktur. Kredit:Georgia Tech Metalliske materialer, der bru
Sporing af atombevægelse i realtid mellem krystalkorn i metallerTing Zhu, professor i maskinteknik ved Georgia Tech, foran sine TEM-billeder af polykrystallinske metaller og en grafisk simulerende atomstruktur. Kredit:Georgia Tech Metalliske materialer, der bru -
 Forskere laver kraftfuld undervandslim inspireret af havbarn og muslingerModelfly monteret med silkebaseret lim. Kredit:Marco Lo Presti, Tufts University Hvis du nogensinde har prøvet at hugge en musling ud af en havmur eller et fjeder af bunden af en båd, du vil for
Forskere laver kraftfuld undervandslim inspireret af havbarn og muslingerModelfly monteret med silkebaseret lim. Kredit:Marco Lo Presti, Tufts University Hvis du nogensinde har prøvet at hugge en musling ud af en havmur eller et fjeder af bunden af en båd, du vil for
- Ny undersøgelse af Sebastian Inlet bekræfter sammenhængen mellem havniveau, sandvolumen
- Lodrette målinger af luftforurenende stoffer i byerne Beijing
- Hvad er urushiol?
- Hvordan påvirker sediment økosystemet?
- Hvad anvendes nogle kemiske reaktioner i fremstillingen af papir?
- Er de fleste faste stoffer tætte og svære at komprimere?


