Hvor mange af valenselektronerne bruges til at fremstille sigma -bindinger i ethylacetat?
1. Struktur af ethylacetat
Ethylacetat har følgende struktur:
`` `
O
||
CH3-C-O-CH2-CH3
`` `
2. Valenselektroner
* carbon (c): 4 valenselektroner
* brint (H): 1 Valenselektron
* ilt (O): 6 Valenselektroner
3. Sigma Bonds
Sigma -obligationer er den stærkeste type kovalente binding og dannes af den direkte overlapning af atomiske orbitaler. Lad os tælle Sigma -bindingerne i ethylacetat:
* C-H-obligationer: Der er 6 C-H Sigma-bindinger (3 i hver methylgruppe).
* C-C-obligationer: Der er 2 C-C Sigma-bindinger (en mellem carbonylcarbonet og det tilstødende kulstof og en i ethylgruppen).
* C-O-obligationer: Der er 2 C-O Sigma-bindinger (en mellem carbonylcarbon og ilt og en mellem ilt og ethylgruppen).
Samlede Sigma -obligationer:6 + 2 + 2 =10
4. Valenselektroner i Sigma -obligationer
Hver Sigma -binding involverer 2 valenselektroner (en fra hvert atom, der deltager i bindingen). Derfor er det samlede antal valenselektroner involveret i Sigma -bindinger i ethylacetat:
10 Sigma -obligationer * 2 Valenselektroner/Sigma Bond =20 Valenselektroner
Svar: 20 Valenselektroner bruges til at fremstille sigma -bindinger i ethylacetat.
Sidste artikelHvorfor brintperoxid opbevaret i mørke flasker?
Næste artikelHvor mange ioner er i 0,187 mol Na plus ioner?
 Varme artikler
Varme artikler
-
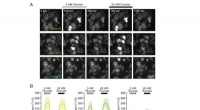 Grønne fluorescerende proteinbaserede glukoseindikatorer til overvågning af glukosemetabolisme i r…A:Billeder af HeLa -celler, der udtrykker Green Glifon50, Grøn Glifon600 og Grøn Glifon4000. Skalaen repræsenterer 20 μm. B:Ændringer i fluorescensintensitet (FI) i HeLa -celler, der udtrykker de tre
Grønne fluorescerende proteinbaserede glukoseindikatorer til overvågning af glukosemetabolisme i r…A:Billeder af HeLa -celler, der udtrykker Green Glifon50, Grøn Glifon600 og Grøn Glifon4000. Skalaen repræsenterer 20 μm. B:Ændringer i fluorescensintensitet (FI) i HeLa -celler, der udtrykker de tre -
 Screen kunne tilbyde bedre sikkerhedstests for nye kemikalierMIT -kemikere har udtænkt en måde at observere overgangstilstanden for den kemiske reaktion, der opstår, når vinylcyanid brydes fra hinanden af en ultraviolet laser. Kredit:Christine Daniloff, MIT
Screen kunne tilbyde bedre sikkerhedstests for nye kemikalierMIT -kemikere har udtænkt en måde at observere overgangstilstanden for den kemiske reaktion, der opstår, når vinylcyanid brydes fra hinanden af en ultraviolet laser. Kredit:Christine Daniloff, MIT -
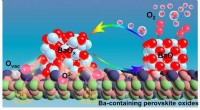 Mekanisme for oxygenaktivering på bariumholdige perovskitmaterialerOxygenaktiveringsmekanisme på Ba-holdige perovskitoxider. Kredit:Zhu Yue Et forskerhold ledet af prof. Yang Weishen og prof. Zhu Xuefeng fra Dalian Institute of Chemical Physics (DICP) fra det kine
Mekanisme for oxygenaktivering på bariumholdige perovskitmaterialerOxygenaktiveringsmekanisme på Ba-holdige perovskitoxider. Kredit:Zhu Yue Et forskerhold ledet af prof. Yang Weishen og prof. Zhu Xuefeng fra Dalian Institute of Chemical Physics (DICP) fra det kine -
 Følsom ny test påviser antistoffer mod SARS-CoV-2 på kun 10 minutterEn ny lateral flow immunoassay kan påvise antistoffer mod SARS-CoV-2, som vises som en lys orange streg, når de placeres på en fluorescenslæser (højre). Kredit:Guanfeng Lin Da COVID-19-kurven vise
Følsom ny test påviser antistoffer mod SARS-CoV-2 på kun 10 minutterEn ny lateral flow immunoassay kan påvise antistoffer mod SARS-CoV-2, som vises som en lys orange streg, når de placeres på en fluorescenslæser (højre). Kredit:Guanfeng Lin Da COVID-19-kurven vise
- Hvor slem er strålingen på Mars?
- Hvad er et LRAD? Forklarer de soniske våben, politiet bruger til kontrol af publikum og kommunikati…
- Afhænger gravitations- og elektriske kræfter af en fysisk egenskab ved genstande?
- Alkymister af cellemiljøet
- En opdagelse af et sort hul kunne tvinge os til at genoverveje, hvordan galakser opstod
- Sublimeringen af fast is sker lige så hurtigt som fordampningen af flydende vand


