Type obligationer brudt, når kalium koger?
Her er hvorfor:
* Metallisk binding: I metaller delokaliseres de ydre valenselektroner og danner et "hav" af elektroner, der deles mellem alle atomer. Dette skaber stærke attraktive kræfter mellem de positivt ladede metalioner og det negativt ladede elektronhav, hvilket resulterer i metallisk binding.
* kogning: Når et stof koger, overvindes kræfterne, der holder molekylerne eller atomerne sammen. I tilfælde af kalium leveres der nok energi til at bryde de metalliske bindinger mellem kaliumatomerne, hvilket giver dem mulighed for at skifte fra væsken til den gasformige tilstand.
Sidste artikelHvad er antallet af elektroner i titanium?
Næste artikelHvad katalyserer kemisk reaktion?
 Varme artikler
Varme artikler
-
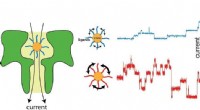 Med nanopore sansning, fysikforskere opdager subtile ændringer i enkelte partiklerResistiv puls nanopore sensing er baseret på ideen om, at små ændringer i strømmen, der bevæger sig gennem en nanopore (grøn, venstre) kan bruges til at lære om molekyler indeholdt. Forskerne var i st
Med nanopore sansning, fysikforskere opdager subtile ændringer i enkelte partiklerResistiv puls nanopore sensing er baseret på ideen om, at små ændringer i strømmen, der bevæger sig gennem en nanopore (grøn, venstre) kan bruges til at lære om molekyler indeholdt. Forskerne var i st -
 Aerogel:Fremtidens mikrostrukturmaterialeFor at demonstrere, at fine aerogelstrukturer kan fremstilles i 3D-print, forskerne trykte en lotusblomst lavet af aerogel. Kredit:Empa Aerogel er en fremragende termisk isolator. Indtil nu, imidl
Aerogel:Fremtidens mikrostrukturmaterialeFor at demonstrere, at fine aerogelstrukturer kan fremstilles i 3D-print, forskerne trykte en lotusblomst lavet af aerogel. Kredit:Empa Aerogel er en fremragende termisk isolator. Indtil nu, imidl -
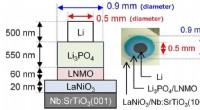 Udvidelse af grænserne for Li-ion-batterier – elektroder til hel-solid-state batterierBatterierne blev fremstillet ved at stable forskellige lag via tynd-film aflejringsmetoder. LNMO/Li 3 PO 4 grænsefladen viste spontan migration af Li-ioner og havde en hidtil uset lav modstand. Kr
Udvidelse af grænserne for Li-ion-batterier – elektroder til hel-solid-state batterierBatterierne blev fremstillet ved at stable forskellige lag via tynd-film aflejringsmetoder. LNMO/Li 3 PO 4 grænsefladen viste spontan migration af Li-ioner og havde en hidtil uset lav modstand. Kr -
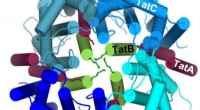 Biokemikere undersøger transporten af store proteiner gennem bakterielle cellemembranerFire TatC-molekyler (blå) danner en cirkel omkring fire TatB-molekyler (grøn) for at danne et hulrum i midten, hvori det protein, der skal transporteres, kan indsættes nedefra. Kredit: Journal of Biol
Biokemikere undersøger transporten af store proteiner gennem bakterielle cellemembranerFire TatC-molekyler (blå) danner en cirkel omkring fire TatB-molekyler (grøn) for at danne et hulrum i midten, hvori det protein, der skal transporteres, kan indsættes nedefra. Kredit: Journal of Biol
- Hvem er kulstof og silicium tilbageholdende med at danne ioniske bindinger?
- Hvordan bakterier overlever miljøer med lavt iltindhold
- Hvor kommer farverne fra i nord- og sydlys?
- Hvad er sammenbruddet af en masse jord eller klipper fra bjerget kaldet?
- Startups, old-line bilproducenter sigter mod at tage bid af Tesla
- Forskel mellem opløselighed og molaritet


