Klorgas reagerer med vandigt kaliumiodid til dannelse af fast jod og chlorid?
cl₂ (g) + 2ki (aq) → i₂ (s) + 2kcl (aq)
Forklaring:
* klorgas (CL₂) er en mere reaktiv halogen end jod. Dette betyder, at det kan fortrænge jod fra dets forbindelse.
* Kaliumiodid (KI) opløses i vand og danner en vandig opløsning.
* Kloren reagerer med iodidionerne (I-) i opløsning, danner jod (I₂), der udfældes som et fast stof.
* kaliumchlorid (KCL) forbliver opløst i opløsning.
Nøgleobservationer:
* Du vil se et brun-lilla fast (jod) dannes i opløsningen.
* Opløsningen kan også blive lidt sur på grund af dannelsen af saltsyre (HCI).
Fortæl mig, hvis du har flere spørgsmål om denne reaktion eller andre kemiske reaktioner!
 Varme artikler
Varme artikler
-
 Identifikation af designermedicin taget af overdosispatienterLægemidler frigivet fra testpatronen (i midten) identificeres af et massespektrometer (venstre). Kredit:Greta Ren Overdosering af stoffer tager en enorm vejafgift på folkesundheden, med potente sy
Identifikation af designermedicin taget af overdosispatienterLægemidler frigivet fra testpatronen (i midten) identificeres af et massespektrometer (venstre). Kredit:Greta Ren Overdosering af stoffer tager en enorm vejafgift på folkesundheden, med potente sy -
 Tilsæt bare vand:Enkelt trin øger polymerers evne til at filtrere kuldioxid fra blandede gasserKredit:NC State Et internationalt team af forskere har fundet ud af, at det kan øge en eksisterende polymers evne til selektivt at fjerne kuldioxid (CO 2 ) ud af gasblandinger ved først at nedsæ
Tilsæt bare vand:Enkelt trin øger polymerers evne til at filtrere kuldioxid fra blandede gasserKredit:NC State Et internationalt team af forskere har fundet ud af, at det kan øge en eksisterende polymers evne til selektivt at fjerne kuldioxid (CO 2 ) ud af gasblandinger ved først at nedsæ -
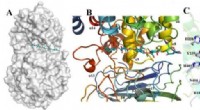 Strukturer i tang kaster lys over bæredygtighedOverfladerepræsentation og substratbindingsrille på Dp0100 Kredit:JI Shiqi Brunalger er ikke bare tang, der flyder i havet og floker svømmernes fødder - de indeholder også en hemmelighed. I sin ce
Strukturer i tang kaster lys over bæredygtighedOverfladerepræsentation og substratbindingsrille på Dp0100 Kredit:JI Shiqi Brunalger er ikke bare tang, der flyder i havet og floker svømmernes fødder - de indeholder også en hemmelighed. I sin ce -
 Ny biokemisk vej, der kan udvikle mere modstandsdygtige afgrødesorterKredit:CC0 Public Domain Forskere fra Institut for Plantevidenskab, University of Oxford, har opdaget en ny biokemisk vej i planter, som de har kaldt CHLORAD. Ved at manipulere CHLORAD-vejen, for
Ny biokemisk vej, der kan udvikle mere modstandsdygtige afgrødesorterKredit:CC0 Public Domain Forskere fra Institut for Plantevidenskab, University of Oxford, har opdaget en ny biokemisk vej i planter, som de har kaldt CHLORAD. Ved at manipulere CHLORAD-vejen, for


