Hvad er nedbrydningen af nitrogen, der indeholder molekyler til ammoniak?
Her er hvorfor:
* ammoniak er et meget stabilt molekyle: Det er vanskeligt at nedbrydes i dets bestanddele (nitrogen og brint).
* nitrogenholdige molekyler er forskellige: De varierer meget i deres struktur og binding, hvilket gør en enkelt nedbrydningsvej umulig.
I stedet for nedbrydning overvejer vi normalt følgende:
* nitrogenfiksering: Dette er den proces, hvormed atmosfærisk nitrogen (N₂) omdannes til ammoniak (NH₃). Dette er en vigtig proces for livet på jorden, da det gør kvælstof til rådighed for planter og i sidste ende alle levende organismer.
* Biologisk nitrogenfiksering: Visse bakterier omdanner atmosfærisk nitrogen til ammoniak ved hjælp af enzymer.
* Industriel nitrogenfiksering: Haber-Bosch-processen bruger højt tryk og temperatur til at omdanne nitrogen og brint til ammoniak.
* Kemisk syntese: Ammoniak kan produceres fra andre nitrogenholdige molekyler gennem forskellige kemiske reaktioner.
Eksempel:
Du tænker måske på nedbrydning af organiske forbindelser indeholdende nitrogen. Dette producerer dog ikke direkte ammoniak. I stedet opdeles disse forbindelser i forskellige produkter, hvoraf nogle kan indeholde nitrogen i forskellige former, såsom:
* aminer: Disse forbindelser indeholder et nitrogenatom, der er direkte bundet til et carbonatom.
* nitriles: Disse forbindelser indeholder et carbonatom, der er tredobbeltbundet til et nitrogenatom.
for at opsummere:
Der er ikke en simpel "nedbrydning" af nitrogenholdige molekyler til ammoniak. Det er mere nøjagtigt at overveje nitrogenfiksering eller kemisk syntese til ammoniakproduktion.
Sidste artikelHvilket ikke-jernholdigt metal bruges til batteribeholder?
Næste artikelHvorfor renser syrer kobbermønter bedst?
 Varme artikler
Varme artikler
-
 Sådan får du ledende geler til at klæbe, når de er våde(A) Billede af en lap-shear test opsætning. Billedkredit:Hyunwoo Yuk, MIT. (B) Billede af klæbemiddelsvigt under en lap-shear test af en våd PEDOT:PSS klæbet på et uberørt glas eller et uberørt glas m
Sådan får du ledende geler til at klæbe, når de er våde(A) Billede af en lap-shear test opsætning. Billedkredit:Hyunwoo Yuk, MIT. (B) Billede af klæbemiddelsvigt under en lap-shear test af en våd PEDOT:PSS klæbet på et uberørt glas eller et uberørt glas m -
 Strontiumtitanats nye egenskaber er vigtige for elektronikforskningEPR-spektre for de (001)-orienterede enkeltkrystalprøver med form som en stang og en plade af STO:Fe3+ ved T =300 K (a) og af en plade af STO:Mn4+ ved T =150 K (b) . Orienteringerne af prøverne i forh
Strontiumtitanats nye egenskaber er vigtige for elektronikforskningEPR-spektre for de (001)-orienterede enkeltkrystalprøver med form som en stang og en plade af STO:Fe3+ ved T =300 K (a) og af en plade af STO:Mn4+ ved T =150 K (b) . Orienteringerne af prøverne i forh -
 Økolim kan erstatte skadelige klæbemidler i træbyggeriKredit:Aalto Universitet Forskere ved Aalto Universitetet har udviklet en biobaseret klæbemiddel, der kan erstatte formaldehydholdige klæbemidler i træbyggeri. Det vigtigste råmateriale i den nye l
Økolim kan erstatte skadelige klæbemidler i træbyggeriKredit:Aalto Universitet Forskere ved Aalto Universitetet har udviklet en biobaseret klæbemiddel, der kan erstatte formaldehydholdige klæbemidler i træbyggeri. Det vigtigste råmateriale i den nye l -
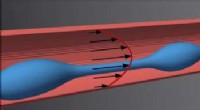 Fysikere opdager mekanismer til dannelse af blodpladerIndividuelle dråber dannes af en aflang fingerformet celle (blå) i blodgennemstrømningen. Hver dråbe udvikler sig til en blodplade. Billede:UBT / Christian Bächer. Kredit:University of Bayreuth Bl
Fysikere opdager mekanismer til dannelse af blodpladerIndividuelle dråber dannes af en aflang fingerformet celle (blå) i blodgennemstrømningen. Hver dråbe udvikler sig til en blodplade. Billede:UBT / Christian Bächer. Kredit:University of Bayreuth Bl
- Når en remskive knækker og falder på gulvet, hvilken ændring i kraft kaldes dette?
- Sådan laver du en elektrisk motor ved hjælp af et 9V-batteri
- I den fjerne fremtid, stjernernes forbiflyvninger vil fuldstændig demontere solsystemet
- Hvis en kurve med en radius på 60 m er korrekt skrånende for bil, der kører kmh, hvad skal den st…
- 3D-scanning af sandstensfossiler afslører den ældste kendte registrering af paddespor i Storbritan…
- At drage omsorg for samfundet for at slå coronavirus afspejler indfødte ideer om et godt liv


