Hvor mange gram N2 skal reagere på form 1,7 ammoniak NH3?
1. Skriv den afbalancerede kemiske ligning:
N₂ (G) + 3H₂ (G) → 2NH₃ (G)
2. Bestem molforholdet:
Den afbalancerede ligning fortæller os, at 1 mol N₂ reagerer på at producere 2 mol NH₃.
3. Konverter gram af NH₃ til mol:
* Find den molære masse af NH₃:(14,01 g/mol N) + (3 * 1,01 g/mol H) =17,04 g/mol
* Opdel massen af NH₃ med dens molære masse:1,7 g NH₃ / 17,04 g / mol =0,1 mol NH₃
4. Beregn mol af N₂:
* Brug molforholdet fra den afbalancerede ligning:(0,1 mol NH₃) * (1 mol N₂ / 2 mol NH₃) =0,05 mol N₂
5. Konverter mol n₂ til gram:
* Find den molære masse af N₂:2 * 14,01 g/mol =28,02 g/mol
* Multiplicer mol af N₂ med dens molære masse:0,05 mol N₂ * 28,02 g/mol =1,4 g N₂
Derfor skal 1,4 gram N₂ reagere på form 1,7 gram NH₃.
Sidste artikelHvordan balanserer du ligningen mellem silicium og ilt?
Næste artikelEr Stoddard opløsningsmiddel det samme som parafin?
 Varme artikler
Varme artikler
-
 Skinnende molekyler skelner mellem proteiner i hjernenHjernevæv med Alzheimers patologi, farvet med et af de nye tau-specifikke molekyler (orange) og et af de molekyler, der tidligere er udviklet af gruppen ved LiU (blå). Billedet er taget i et fluoresce
Skinnende molekyler skelner mellem proteiner i hjernenHjernevæv med Alzheimers patologi, farvet med et af de nye tau-specifikke molekyler (orange) og et af de molekyler, der tidligere er udviklet af gruppen ved LiU (blå). Billedet er taget i et fluoresce -
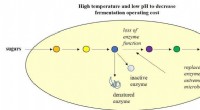 Forskere konstruerer hårdere mikrober for at forbedre bioproduktion af brændstoffer, kemikalierForskere arbejder på at identificere og producere robuste enzymer, der kan erstatte andre enzymer, der nedbrydes i gæringen af biobaserede brændstoffer og kemikalier. Kredit:Laura Jarboe. Travl,
Forskere konstruerer hårdere mikrober for at forbedre bioproduktion af brændstoffer, kemikalierForskere arbejder på at identificere og producere robuste enzymer, der kan erstatte andre enzymer, der nedbrydes i gæringen af biobaserede brændstoffer og kemikalier. Kredit:Laura Jarboe. Travl, -
 Ufuldkommenhed er OK for bedre MOF'erLavdosis højopløsningstransmissionselektronmikroskopi gør det muligt at identificere forskellige defekte strukturer i et metal-organisk rammemateriale og afslører deres vigtige roller i katalytiske ap
Ufuldkommenhed er OK for bedre MOF'erLavdosis højopløsningstransmissionselektronmikroskopi gør det muligt at identificere forskellige defekte strukturer i et metal-organisk rammemateriale og afslører deres vigtige roller i katalytiske ap -
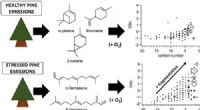 Bladlusstressede fyrretræer viser forskellig sekundær organisk aerosoldannelseKredit:American Chemical Society Planter udsender gasser, kaldet flygtige organiske forbindelser (VOCer), der kommer ind i atmosfæren, hvor de kan interagere med andre naturlige og menneskeskabte
Bladlusstressede fyrretræer viser forskellig sekundær organisk aerosoldannelseKredit:American Chemical Society Planter udsender gasser, kaldet flygtige organiske forbindelser (VOCer), der kommer ind i atmosfæren, hvor de kan interagere med andre naturlige og menneskeskabte
- Hvordan dannede kontinentalsokkelen?
- Millennials håber at nå livets milepæle i samme alder som andre generationer, siger undersøgelse
- Hvad sker der med stemmen fra en dykker, der trækker vejret i blandingen ilt og helium?
- Boeing, flyselskaber står over for en hård vej efter 737 MAX-grundstødning
- Hvis fyrretræerne forsvinder, kan det så stadig hedde Big Pine Key?
- Er energi et substantiv adjektiv eller verb?


