Hvad er energifaktor for ammoniumnitratopløsning ioner i vand?
Her er hvorfor:
* endotermisk vs. eksotermisk: Opløsning af ammoniumnitrat i vand er en endotermisk behandle. Dette betyder, at varme absorberes fra omgivelserne, hvilket får løsningen til at føle sig kold.
* entalpiændring (ΔH): Enthalpyændringen til opløsning af ammoniumnitrat i vand er positiv . En positiv ΔH indikerer en endotermisk reaktion.
* Faktorer, der påvirker entalpiændring: Enthalpyændringen af opløsende ammoniumnitrat i vand påvirkes af:
* gitterenergi: Energien, der holder ionerne sammen i det faste ammoniumnitrat.
* Hydratiseringsenergi: Energien frigivet, når ionerne er omgivet af vandmolekyler.
Beregning af entalpiændringen:
Du kan finde enthalpiændringen af opløsende ammoniumnitrat i vand eksperimentelt eller slå det op i en referencetabel.
Bemærk: Det er vigtigt at skelne mellem "entalpiændring" og "energifaktor." Enthalpy -ændringen kvantificerer varmestrømmen, mens "energifaktor" er et mindre specifikt udtryk, der kan have forskellige betydninger i forskellige sammenhænge.
Sidste artikelHvad er to egenskaber ved forbrændingsreaktioner?
Næste artikelHvad er den molekylære diameter af benzen?
 Varme artikler
Varme artikler
-
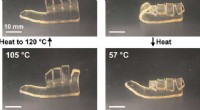 Tuning af frontal polymerisering til forskellige materialegenskaberBillederne illustrerer ændringen i polymerform afhængigt af glasovergangstemperaturen. Kredit:Autonomous Materials Systems Group. Forskere fra University of Illinois i Urbana-Champaign har forbedr
Tuning af frontal polymerisering til forskellige materialegenskaberBillederne illustrerer ændringen i polymerform afhængigt af glasovergangstemperaturen. Kredit:Autonomous Materials Systems Group. Forskere fra University of Illinois i Urbana-Champaign har forbedr -
 Nyt center til at erstatte olie og gas med bæredygtig kemiKredit:Københavns Universitet Mange af de ting, der omgiver os, er kemisk afledt af fossil gas og olie - fra vaskepulver til telefoner til lægemidler. Som sådan, kemi bidrager til CO 2 emissione
Nyt center til at erstatte olie og gas med bæredygtig kemiKredit:Københavns Universitet Mange af de ting, der omgiver os, er kemisk afledt af fossil gas og olie - fra vaskepulver til telefoner til lægemidler. Som sådan, kemi bidrager til CO 2 emissione -
 Nye sensorer kan muliggøre en mere overkommelig påvisning af forurening og sygdommeKredit:American Chemical Society Når det kommer til at teste for kræft, miljøforurening og fødevareforurenende stoffer, traditionelle sensorer kan hjælpe. Udfordringerne er, at de ofte er omfangsr
Nye sensorer kan muliggøre en mere overkommelig påvisning af forurening og sygdommeKredit:American Chemical Society Når det kommer til at teste for kræft, miljøforurening og fødevareforurenende stoffer, traditionelle sensorer kan hjælpe. Udfordringerne er, at de ofte er omfangsr -
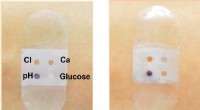 Biosensorbandage opsamler og analyserer svedBiosensorbandage før (venstre) og efter (højre) svedsekretion. Kredit:American Chemical Society Ligesom andre biovæsker, sved indeholder et væld af informationer om, hvad der foregår inde i kroppe
Biosensorbandage opsamler og analyserer svedBiosensorbandage før (venstre) og efter (højre) svedsekretion. Kredit:American Chemical Society Ligesom andre biovæsker, sved indeholder et væld af informationer om, hvad der foregår inde i kroppe
- Kan det private rum overleve to eksplosioner på fire dage? (Opdatering)
- Er kraften af tiltrækning stærkere i molekyler en fast eller væske?
- Hvilke levende og ikke -levende ting i et skovøkosystem?
- Storbritannien har et højere niveau af regional ulighed end noget andet stort velhavende land
- Hvornår sendte rumfartøjet først tilbage data og billeder fra planeterne?
- Forskere finder sammenhæng mellem atlantiske orkaner og vejrsystemet i Østasien


