Hvad er en stabil forbindelse?
Her er nogle vigtige aspekter af stabile forbindelser:
* termodynamisk stabilitet: De har en lavenergitilstand, hvilket betyder, at de er mindre tilbøjelige til at gennemgå reaktioner, der vil frigive energi.
* kinetisk stabilitet: De reagerer langsomt eller slet ikke med andre stoffer, selvom disse reaktioner ville være energisk gunstige.
* Kemisk inertitet: De er generelt ureaktive og deltager ikke let i kemiske reaktioner.
* modstand mod nedbrydning: De modstår at bryde ned til enklere stoffer.
Eksempler på stabile forbindelser:
* vand (H₂O): En meget stabil forbindelse, der findes i flydende form ved stuetemperatur.
* kuldioxid (co₂): En stabil forbindelse, der findes i atmosfæren.
* natriumchlorid (NaCl): Tabel salt er en stabil forbindelse, der ikke let nedbrydes eller reagerer med andre stoffer.
* diamant (c): En meget stabil allotrop af kulstof med en stærk kovalent netværksstruktur.
Faktorer, der påvirker stabiliteten:
* obligationsstyrke: Stærkere bindinger mellem atomer fører til større stabilitet.
* Elektronkonfiguration: Forbindelser med stabile elektronkonfigurationer har en tendens til at være mere stabile.
* entropi: Forbindelser med lavere entropi (mere orden) er generelt mere stabile.
Bemærk: Stabilitet er relativ og afhænger af de specifikke betingelser. En forbindelse, der betragtes som stabil under normale forhold, kan blive ustabile under ekstreme forhold, såsom høje temperaturer, tryk eller tilstedeværelsen af katalysatorer.
Sidste artikelHvor mange carbonatomer tager det for at svare til 12.011 gram?
Næste artikelHvilken slags element reagerer metaller med?
 Varme artikler
Varme artikler
-
 Forandrende resultater skubber 3D-print til den molekylære grænseKredit:University of Nottingham New University of Nottingham forskning beviser, at avancerede materialer, der indeholder molekyler, der skifter tilstand som reaktion på miljøstimuli såsom lys, kan
Forandrende resultater skubber 3D-print til den molekylære grænseKredit:University of Nottingham New University of Nottingham forskning beviser, at avancerede materialer, der indeholder molekyler, der skifter tilstand som reaktion på miljøstimuli såsom lys, kan -
 Forskere anvender kemiske værktøjer til at opdage kræftfremkaldende proteinerYekaterina Kovalyova. Kredit:Yale University Forskere ved Yales Microbial Sciences Institute har taget et vigtigt skridt i vores forståelse af, hvordan infektion ændrer proteiner på en måde, der fr
Forskere anvender kemiske værktøjer til at opdage kræftfremkaldende proteinerYekaterina Kovalyova. Kredit:Yale University Forskere ved Yales Microbial Sciences Institute har taget et vigtigt skridt i vores forståelse af, hvordan infektion ændrer proteiner på en måde, der fr -
 Slikker en Tootsie Roll -sensor for at overvåge sundhedEn elektrode fremstillet med en støbt Tootsie Roll og aluminiumsrør kan hjælpe med at overvåge ægløsningstilstand og nyresundhed. Kredit:Tilpasset fra ACS Applied Materials &Interfaces 2021 Engang
Slikker en Tootsie Roll -sensor for at overvåge sundhedEn elektrode fremstillet med en støbt Tootsie Roll og aluminiumsrør kan hjælpe med at overvåge ægløsningstilstand og nyresundhed. Kredit:Tilpasset fra ACS Applied Materials &Interfaces 2021 Engang -
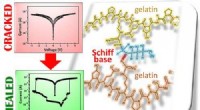 Selvreparerende gelatinebaseret film kan være et smart træk for elektronikKredit:American Chemical Society At tabe en mobiltelefon kan nogle gange forårsage overfladiske revner. Men andre gange, enheden kan helt stoppe med at fungere, fordi der udvikles brud i det mater
Selvreparerende gelatinebaseret film kan være et smart træk for elektronikKredit:American Chemical Society At tabe en mobiltelefon kan nogle gange forårsage overfladiske revner. Men andre gange, enheden kan helt stoppe med at fungere, fordi der udvikles brud i det mater
- Hvilke udtryk beskriver to atomer, når de danner en binding, hvor Electorns overføres fuldstændig…
- NASA ser november for opsendelsesforsøg med måneraket
- Hvilket udtryk beskriver bedst klimaet i Iran Tropical Semiarid eller Rainy?
- Sådan beregnes aluminium Weight
- Er nitrogen i luften skadeligt?
- Hvilke to elementer undersøgte Dalton?


