Hvad er reaktionen, når jern III acetat lægger i vand?
1. Opløsning og ionisering:
* Jern (III) acetat opløses i vand og adskiller sig i dets bestanddele:
Fe (CH 3 COO) 3 (S) → Fe 3+ (aq) + 3ch 3 COO - (aq)
2. Hydrolyse af jern (III) ioner:
* Iron (III) ioner (Fe 3+ ) Reager med vandmolekyler, danner hydratiseret jern (III) ioner og frigiver hydroniumioner (H 3 O + ):
Fe 3+ (aq) + h 2 O (l) ⇌ [Fe (h 2 O) 6 ] 3+ (aq) + h 3 O + (aq)
3. Hydrolyse af acetationer:
* Acetationerne (CH 3 COO - ) kan også reagere med vand, danne eddikesyre (CH 3 COOH) og hydroxidioner (OH - ):
CH 3 COO - (aq) + h 2 O (l) ⇌ ch 3 COOH (aq) + oh - (aq)
4. Ligevægt og pH:
* Disse reaktioner når ligevægt, hvilket resulterer i en let sur opløsning (pH <7) på grund af tilstedeværelsen af hydroniumioner.
5. Dannelse af bundfald:
* Afhængig af koncentrationen af jern (III) acetat og pH -værdien i opløsningen, jern (III) hydroxid (Fe (OH) 3 ) kan udfælde sig som et rødbrunt fast stof.
Sammendrag:
Reaktionen af jern (III) acetat med vand er en kompleks proces, der involverer opløsning, ionisering, hydrolyse og ligevægt. Det endelige resultat afhænger af faktorer som koncentration og pH. Opløsningen vil være lidt sur og kan indeholde et rødbrunt bundfald af jern (III) hydroxid.
Sidste artikelHvad er CO et element eller forbindelse?
Næste artikelHvad er den kemiske forbindelse dannet mellem lithium og svovl?
 Varme artikler
Varme artikler
-
 Undersøgelse afslører indsigt i enzym, der bekæmper en almindelig drivhusgasTre tilstande af modningsapparatet af N2 O-reduktase:Et kompleks af proteinerne NosF (gul), NosY (rød) og NosD (grøn) ændrer sin konformation ved at forbruge biokemisk energi og kan dermed overtage en
Undersøgelse afslører indsigt i enzym, der bekæmper en almindelig drivhusgasTre tilstande af modningsapparatet af N2 O-reduktase:Et kompleks af proteinerne NosF (gul), NosY (rød) og NosD (grøn) ændrer sin konformation ved at forbruge biokemisk energi og kan dermed overtage en -
 Nylon indtager endelig sin plads som et piezoelektrisk tekstilOpløsningsmiddeldesign og elektrospinningsteknik knækker 50 år gammel gåde for at få piezoelektriske nylonfibre. Udarbejdet af K. Maisenbacher. Kredit:Max Planck Institute for Polymer Research Nyl
Nylon indtager endelig sin plads som et piezoelektrisk tekstilOpløsningsmiddeldesign og elektrospinningsteknik knækker 50 år gammel gåde for at få piezoelektriske nylonfibre. Udarbejdet af K. Maisenbacher. Kredit:Max Planck Institute for Polymer Research Nyl -
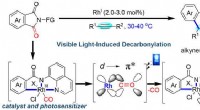 Synligt lys-induceret bifunktionel rhodiumkatalyse udviklet til decarbonylativ kobling af imider med…Lysinduceret bifunktionel rhodiumkatalyse til decarbonylering. Kredit:MIN Xiangting Carbonylgrupper er allestedsnærværende i lægemidler, naturlige produkter, og landbrugskemikalier, især amider. O
Synligt lys-induceret bifunktionel rhodiumkatalyse udviklet til decarbonylativ kobling af imider med…Lysinduceret bifunktionel rhodiumkatalyse til decarbonylering. Kredit:MIN Xiangting Carbonylgrupper er allestedsnærværende i lægemidler, naturlige produkter, og landbrugskemikalier, især amider. O -
 Ny fotoakustisk teknik registrerer gasser på dele-per-quadrillion niveauVed hjælp af en ny teknik kan en enhed detektere gasser, såsom miljøforurenende stoffer, i ekstremt små koncentrationer. Kredit:Gerald Diebold Et team af forskere har fundet en måde at detektere s
Ny fotoakustisk teknik registrerer gasser på dele-per-quadrillion niveauVed hjælp af en ny teknik kan en enhed detektere gasser, såsom miljøforurenende stoffer, i ekstremt små koncentrationer. Kredit:Gerald Diebold Et team af forskere har fundet en måde at detektere s
- Er densiteten af kobber mere end jern?
- Forskere udvikler molekylær rygrad af superslank, bøjelige digitale skærme
- Afbrudt opsendelse af Soyuz-rumfartøjet:hvad vi ved
- Hvad er den gode opfattelse, det er tilbøjeligt eller lodrett at undersøge mikroskop?
- Hvor mange solsystemer vides i øjeblikket at eksistere i universet?
- Hvordan kan tyngdekraften forårsage bevægelse af jordmineraler?


