Hvorfor reageres natriummetal ikke normalt i laboratoriet, selv med en fortyndet syre?
* voldelig reaktion: Reaktionen mellem natriummetal og fortyndet syre (som saltsyre) producerer brintgas og en betydelig mængde varme. Denne reaktion er ekstremt voldelig og kan få natriumet til at eksplodere eller antænde.
* eksplosiv brintgas: Den frigivne brintgas er meget brandfarlig og kan antænde i nærvær af luft, hvilket fører til en brand eller eksplosion.
* Natriumhydroxiddannelse: Reaktionen danner også natriumhydroxid, en stærk base, der er ætsende og kan forårsage alvorlige forbrændinger.
Sikkerhedsmæssige bekymringer:
* brandfare: Den brændbare brintgas produceret udgør en betydelig brandrisiko.
* Eksplosionsfare: Reaktionen kan være eksplosiv, især hvis natriumet er i en pulveriseret eller fint delt tilstand.
* Kemiske forbrændinger: Natriumhydroxid er et ætsende stof, der kan forårsage alvorlige kemiske forbrændinger.
Alternativer:
* Demonstrationer: Hvis reaktionen skal demonstreres, er det bedst at bruge en lille mængde natrium i et kontrolleret miljø med passende sikkerhedsforholdsregler, såsom en røghætte.
* Andre metaller: Andre alkalimetaller som kalium og lithium er endnu mere reaktive end natrium og bør aldrig reageres med syre i en laboratorieindstilling.
Sammenfattende er reaktionen mellem natriummetal og fortyndet syre ekstremt farlig og bør aldrig udføres uden ordentlig sikkerhedsudstyr og ekspertise.
Sidste artikelEr kulilte et surt oxid eller neutralt oxid?
Næste artikelHvilken temperaturskala bruges i den ideelle gasligning?
 Varme artikler
Varme artikler
-
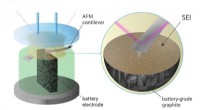 Forskere får et smugkig på en nøgleproces i batterilevetidenEn hovedoversigt over eksperimentet. Kredit:Pavel Odinev / Skoltech Forskere fra Skoltech Center for Energividenskab og Teknologi (CEST) visualiserede dannelsen af en fast elektrolyt-interfase p
Forskere får et smugkig på en nøgleproces i batterilevetidenEn hovedoversigt over eksperimentet. Kredit:Pavel Odinev / Skoltech Forskere fra Skoltech Center for Energividenskab og Teknologi (CEST) visualiserede dannelsen af en fast elektrolyt-interfase p -
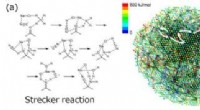 Slå tilbage for at forudsige kemiske reaktioner i flere trinGenererede strukturer og reaktionsvejetværk for de forudsagte reaktionstrin for Strecker-reaktionen (a) og Passerini-reaktionen (b). Hvide pile viser flertrinsvejen svarende til den kendte reaktionsme
Slå tilbage for at forudsige kemiske reaktioner i flere trinGenererede strukturer og reaktionsvejetværk for de forudsagte reaktionstrin for Strecker-reaktionen (a) og Passerini-reaktionen (b). Hvide pile viser flertrinsvejen svarende til den kendte reaktionsme -
 Nyt materiale til at overgå traditionelle oxygenreduktionsreaktionskatalysatorerKredit:CC0 Public Domain En forskergruppe ledet af prof. YANG Minghui ved Ningbo Institute of Materials Technology and Engineering (NIMTE) under det kinesiske videnskabsakademi (CAS) opdagede, at
Nyt materiale til at overgå traditionelle oxygenreduktionsreaktionskatalysatorerKredit:CC0 Public Domain En forskergruppe ledet af prof. YANG Minghui ved Ningbo Institute of Materials Technology and Engineering (NIMTE) under det kinesiske videnskabsakademi (CAS) opdagede, at -
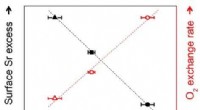 Brændselscellernes levetid maksimeres ved hjælp af en lille mængde metallerKorrelation mellem omfanget af gitterstamme i elektrode, strontiumsegregering, og elektrodereaktion. Kredit:KAIST Brændselsceller er en vigtig fremtidig energiteknologi, der fremstår som miljøvenl
Brændselscellernes levetid maksimeres ved hjælp af en lille mængde metallerKorrelation mellem omfanget af gitterstamme i elektrode, strontiumsegregering, og elektrodereaktion. Kredit:KAIST Brændselsceller er en vigtig fremtidig energiteknologi, der fremstår som miljøvenl
- Når metan forbrænder i nærvær af utilstrækkelige iltprodukter, inkluderer reaktionen kulilte?
- Overraskende opdagelse afslører nye muligheder for halvledermateriale
- Hvilken del af blomsten, hvor mad opbevares som stivelse?
- Hvordan fungerer en katapult?
- Hvilke stoffer produceres i fotosyntese og respiration?
- Ny rapport om pandemiens indvirkning på læringserfaringer for unge med handicap


