Hvordan reagerer hypoklorosyre med jern?
Her er en sammenbrud af reaktionen:
1. Dannelse af jernoxidlag:
* Første reaktion: Oprindeligt reagerer HOCL med jern (Fe) for at danne et tyndt lag jernoxid (Feo) på jernoverfladen. Dette oxidlag er generelt beskyttende og fungerer som en barriere mod yderligere korrosion.
* Ligning: 2Fe + 2HOCl → 2FeO + 2HCl
2. Opløsning af jernoxid:
* sure forhold: Under sure forhold kan HOCl yderligere reagere med jernoxidlaget, opløse det og udsætte frisk jern for yderligere at angribe.
* Ligning: Feo + 2HOCL → FECL2 + H2O + CL2
3. Dannelse af jern (III) ioner:
* Oxidation: Hypochloriske syre fungerer som et oxidationsmiddel, oxiderende jern (II) -ioner (Fe²⁺) til jern (III) -ioner (Fe³⁺).
* Ligning: 2Fe²⁺ + HOCl + H2O → 2Fe³⁺ + Cl⁻ + 3OH⁻
4. Udfældning af jernhydroxider:
* ph -afhængighed: Afhængig af pH i opløsningen kan jern (III) -ioner reagere med hydroxidioner for at danne jernhydroxider (Fe (OH) ₃).
* Ligning: Fe³⁺ + 3OH⁻ → Fe (OH) ₃
samlet reaktion:
Den samlede reaktion af hypochlorosyre med jern er kompleks og kan resultere i forskellige produkter, herunder jern (II) chlorid, jern (III) chlorid og jernhydroxider. De nøjagtige produkter og deres proportioner afhænger af de specifikke betingelser for reaktionen.
Nøglepunkter:
* Korrosion: Reaktionen mellem HOCL og jern kan føre til korrosion af jern, da oxidlaget er opløst og frisk jern udsættes.
* koncentration og pH: Hastigheden og omfanget af reaktionen påvirkes af koncentrationen af HOCl og pH i opløsningen.
* Beskyttelsesfilm: I nogle tilfælde kan reaktionen af HOCl med jern føre til dannelse af beskyttende oxidfilm, der kan hæmme yderligere korrosion.
Det er vigtigt at bemærke, at dette er en forenklet forklaring, og den faktiske reaktionsmekanisme kan være mere kompleks afhængigt af de specifikke betingelser.
 Varme artikler
Varme artikler
-
 Tellurium gør forskellenProfessor Wolfgang Weigand fra det tyske universitet i Jena viser usædvanlige strukturer af tellurforbindelser. Kredit:Anne Günther/Uni Jena Det periodiske system indeholder 118 kemiske grundstoff
Tellurium gør forskellenProfessor Wolfgang Weigand fra det tyske universitet i Jena viser usædvanlige strukturer af tellurforbindelser. Kredit:Anne Günther/Uni Jena Det periodiske system indeholder 118 kemiske grundstoff -
 Mod en miljøvenlig produktion af aktive farmaceutiske ingredienser med en flowreaktorProf. Dr. Harald Gröger arbejder i ONE-FLOW på en måde at producere kemiske forbindelser gennem kombination af bio- og kemokatalyse i flowreaktorer. De kemiske reaktioner udføres f.eks. I moduler med
Mod en miljøvenlig produktion af aktive farmaceutiske ingredienser med en flowreaktorProf. Dr. Harald Gröger arbejder i ONE-FLOW på en måde at producere kemiske forbindelser gennem kombination af bio- og kemokatalyse i flowreaktorer. De kemiske reaktioner udføres f.eks. I moduler med -
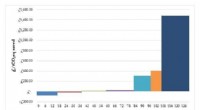 At bringe den kulstofreducerende koldsintringsproces ud af laboratorier og ind i keramikfremstillingKredit:University of Warwick En ny teknoøkonomisk analyse, af et hold ledet af en forsker fra WMG ved University of Warwick, viser, at den energiintensive keramiske industri ville opnå både økonom
At bringe den kulstofreducerende koldsintringsproces ud af laboratorier og ind i keramikfremstillingKredit:University of Warwick En ny teknoøkonomisk analyse, af et hold ledet af en forsker fra WMG ved University of Warwick, viser, at den energiintensive keramiske industri ville opnå både økonom -
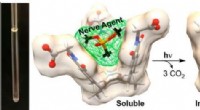 Indfangning af giftige forbindelser med molekylære kurveKredit:Ohio State University Forskere har udviklet designermolekyler, som måske en dag kan opsøge og fange dødelige nervestoffer og andre giftige forbindelser i miljøet – og muligvis i mennesker.
Indfangning af giftige forbindelser med molekylære kurveKredit:Ohio State University Forskere har udviklet designermolekyler, som måske en dag kan opsøge og fange dødelige nervestoffer og andre giftige forbindelser i miljøet – og muligvis i mennesker.


