Hvad inkluderer metaller?
Almindelige egenskaber:
* gode ledere af varme og elektricitet: Dette skyldes den frie bevægelse af elektroner i deres struktur.
* formbar og duktil: De kan hamres i lagner (formbarhed) og trækkes ind i ledninger (duktilitet).
* skinnende (skinnende): De reflekterer let godt og giver dem en egenskab.
* fast ved stuetemperatur: (Bortset fra kviksølv, som er en væske)
* Høj densitet: De er generelt tæt sammenlignet med ikke-metaler.
* høje smelte- og kogepunkter: Dette er igen relateret til den stærke metalliske binding.
Kategorier af metaller:
1. alkalimetaller (gruppe 1): Lithium (Li), natrium (NA), kalium (K), Rubidium (RB), Cesium (CS), Francium (FR)
2. alkaliske jordmetaller (gruppe 2): Beryllium (BE), magnesium (MG), calcium (CA), strontium (SR), barium (BA), radium (RA)
3. Overgangsmetaller: Denne store gruppe inkluderer de fleste af de velkendte metaller som jern (Fe), kobber (Cu), guld (AU), sølv (AG), nikkel (NI) og mange flere.
4. lanthanider: En serie på 15 elementer med lignende egenskaber, der findes i den nederste række af den periodiske tabel.
5. actinider: En anden serie af 15 radioaktive elementer, der også findes i den nederste række.
6. Andre metaller: Denne kategori inkluderer elementer som aluminium (AL), tin (SN), bly (PB) og mere.
Vigtige noter:
* Ikke alle metaller er skabt lige. Nogle er meget reaktive (som alkalimetaller), mens andre er meget ureaktive (som guld).
* Metallers egenskaber kan påvirkes af deres atomstruktur og arrangement.
* Legeringer er blandinger af metaller (eller metaller med andre elementer), der skaber unikke egenskaber.
Husk, at dette kun er et grundlæggende overblik over den enorme og komplekse verden af metaller. Der er meget mere at lære om deres egenskaber, anvendelser og betydning i vores daglige liv.
 Varme artikler
Varme artikler
-
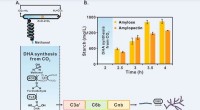 Kinesiske videnskabsmænd rapporterer om stivelsesyntese fra kuldioxidStivelsessyntese via kunstig stivelse anabolsk vej (ASAP) fra kuldioxid. Kredit:TIBCAS Kinesiske videnskabsmænd rapporterede for nylig om en de novo-rute til kunstig stivelsessyntese fra kuldioxid
Kinesiske videnskabsmænd rapporterer om stivelsesyntese fra kuldioxidStivelsessyntese via kunstig stivelse anabolsk vej (ASAP) fra kuldioxid. Kredit:TIBCAS Kinesiske videnskabsmænd rapporterede for nylig om en de novo-rute til kunstig stivelsessyntese fra kuldioxid -
 Fidget spinner som centrifuge adskiller blodplasmaKredit:American Chemical Society Nogle mennesker bruger fidget spinners - flade, legetøj med flere flige med et kugleleje i midten - for at sprede nervøs energi eller hvirvle stress væk. Nu, forsk
Fidget spinner som centrifuge adskiller blodplasmaKredit:American Chemical Society Nogle mennesker bruger fidget spinners - flade, legetøj med flere flige med et kugleleje i midten - for at sprede nervøs energi eller hvirvle stress væk. Nu, forsk -
 Smarte polymerer omdanner elektrisk energi til mekanisk arbejdeKredit:Swiss Federal Laboratories for Materials Science and Technology CT-systemer, et spin-off af Empa, og Daetwyler, den schweiziske specialist i tætningsløsninger, partner til at markedsføre og
Smarte polymerer omdanner elektrisk energi til mekanisk arbejdeKredit:Swiss Federal Laboratories for Materials Science and Technology CT-systemer, et spin-off af Empa, og Daetwyler, den schweiziske specialist i tætningsløsninger, partner til at markedsføre og -
 Bedre termoelektriske egenskaber opnået i n-type kompositTEM-mikrofotografier til kompositprøve fBi 2 Te 2.7 Se 0,3 med f =0,3 vol%. Kredit:Bushra Jabar For nylig, et forskerhold fra Institute of Solid State Physics, Hefei Institutes of Physical S
Bedre termoelektriske egenskaber opnået i n-type kompositTEM-mikrofotografier til kompositprøve fBi 2 Te 2.7 Se 0,3 med f =0,3 vol%. Kredit:Bushra Jabar For nylig, et forskerhold fra Institute of Solid State Physics, Hefei Institutes of Physical S
- Sådan gør du lyse kvanteprikker endnu lysere
- Hybrid nanostruktur med ekstrem lysabsorbering ser lovende ud for fotovoltaik
- De to vigtigste sæt reaktioner, der er involveret i fotosyntesen, er?
- Hvornår forekom kerneenergi?
- Skyderi i Toronto - tabets psykologi, frygt og identitet
- Hvorfor producerer elementer lys?


