Hvorfor skal reaktionen mellem zink og saltsyre udføres i en røghætte væk fra nøgen flamme?
1. Hydrogengasproduktion:
* Reaktionen producerer brintgas (H₂), som er meget brandfarlig og eksplosiv i nærvær af luft.
* En nøgen flamme kunne antænde brintgassen, hvilket fører til en potentielt farlig eksplosion.
* Udførelse af reaktionen i en røghætte sikrer korrekt ventilation, hvilket gør det muligt for brintgassen at sprede sikkert.
2. Giftige dampe:
* Reaktionen producerer også dampe af saltsyre (HCI), som er meget ætsende og irriterende for respirationssystemet.
* Indånding af disse dampe kan forårsage luftvejsproblemer og andre sundhedsmæssige problemer.
* En røghætte giver beskyttelse ved at fange og fjerne disse giftige dampe.
3. Varmeproduktion:
* Reaktionen er eksoterm, hvilket betyder, at den frigiver varme.
* Hvis reaktionen ikke kontrolleres, kan den genererede varme forårsage, at opløsningen koger eller endda antænder den brandfarlige brintgas.
* En røghætte giver mulighed for bedre varmeafledning og kontrol af reaktionstemperaturen.
4. Sikkerhedsforholdsregler:
* Udførelse af reaktionen i en røghætte og væk fra nøgen flamme er en standard sikkerhedsforanstaltning i kemi -laboratorier.
* Det sikrer beskyttelse af både eksperimentatoren og det omgivende miljø.
I resumé er det afgørende for sikkerhed på grund af produktionen af brændbar brintgas, giftige dampe og varmeproduktion under reaktionen under reaktionen under reaktionen under reaktionen.
Sidste artikelKogepunktet for hydrogensulfid lidt højere end selenid?
Næste artikelMassen af et iltmolekyle er?
 Varme artikler
Varme artikler
-
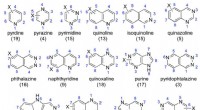 Mod en bedre forståelse af struktur-metabolisme-forhold i human aldehydoxidase (opdatering)Eksempler på de undersøgte azaaromatiske stilladser:antallet af testede forbindelser er angivet i parentes. Kredit:(c) Procedurer fra National Academy of Sciences (2017). DOI:10.1073/pnas.1618881114
Mod en bedre forståelse af struktur-metabolisme-forhold i human aldehydoxidase (opdatering)Eksempler på de undersøgte azaaromatiske stilladser:antallet af testede forbindelser er angivet i parentes. Kredit:(c) Procedurer fra National Academy of Sciences (2017). DOI:10.1073/pnas.1618881114 -
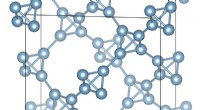 Ultralet aluminium:Kemikere rapporterer gennembrud inden for materialedesignSkematisk afbildning af en supertetrahedral aluminiumkrystalstruktur. Forskere fra Utah State University, USA og Southern Federal University, Rusland, beregningsmæssigt designet en ny, metastabil, ult
Ultralet aluminium:Kemikere rapporterer gennembrud inden for materialedesignSkematisk afbildning af en supertetrahedral aluminiumkrystalstruktur. Forskere fra Utah State University, USA og Southern Federal University, Rusland, beregningsmæssigt designet en ny, metastabil, ult -
 Forskere afslører nye forståelser af syntetiske genkredsløbTian og Wangs forskning afslører ny indsigt om de komplekse forhold mellem syntetiske genkredsløb og cellerne, der er vært for dem. Kredit:Xiaojun Tian/ASU Nylige opdagelser fra to forskerhold i I
Forskere afslører nye forståelser af syntetiske genkredsløbTian og Wangs forskning afslører ny indsigt om de komplekse forhold mellem syntetiske genkredsløb og cellerne, der er vært for dem. Kredit:Xiaojun Tian/ASU Nylige opdagelser fra to forskerhold i I -
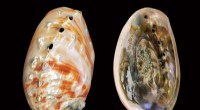 Teknik afslører dybere indsigt i sammensætningen af perlemor, et naturmaterialeDet ydre lag af en abaloneskal, set her, poleres indtil det perlemorlag er blottet. Forskere ved MIT har korreleret mikro-indentation og piezo-Raman-resultater for at evaluere og kvantificere mængden
Teknik afslører dybere indsigt i sammensætningen af perlemor, et naturmaterialeDet ydre lag af en abaloneskal, set her, poleres indtil det perlemorlag er blottet. Forskere ved MIT har korreleret mikro-indentation og piezo-Raman-resultater for at evaluere og kvantificere mængden
- Top 10 rumkonspirationsteorier
- I hvilke dyr når ilt alle celler gennem diffusionsprocessen?
- At studere kølvandet på reflekterede chokbølger afslører kaskaden af kemiske reaktioner involv…
- Mere end halvdelen af unge amerikanere bor hos forældre
- Hvad ioniserede universet?
- Hvordan er hydrosfæren og kryosfæren forskellige?


