Hvorfor er smeltet calciumchlorid ledende?
* ionisk forbindelse: Calciumchlorid er en ionisk forbindelse, hvilket betyder, at det dannes af den elektrostatiske tiltrækning mellem positivt ladede calciumioner (Ca²⁺) og negativt ladede chloridioner (CL⁻).
* solid tilstand: I fast tilstand holdes disse ioner stift i en krystalgitter, hvilket forhindrer dem i at bevæge sig frit. Dette er grunden til, at fast calciumchlorid er en dårlig leder.
* smeltet tilstand: Når calciumchlorid smeltes, overvindes de stærke elektrostatiske kræfter, der holder ionerne sammen. Ionerne kan frit bevæge sig tilfældigt inden i væsken.
* Elektrisk ledningsevne: Når et elektrisk potentiale påføres på tværs af det smeltede calciumchlorid, migrerer de frie calciumioner mod den negative elektrode (katode), og de frie chloridioner migrerer mod den positive elektrode (anode). Denne bevægelse af ladede partikler udgør en elektrisk strøm.
I resuméet skyldes konduktiviteten af smeltet calciumchlorid dissocieringen af dets bestanddele i en mobil, ladningsførende væske.
Sidste artikelHvad er rollen som thionylchlorid i rektion methanol med L-serin?
Næste artikelKemisk formel til bly II perchlorat?
 Varme artikler
Varme artikler
-
 Kontinuerlig og stabil lasning opnået fra billige perovskitter ved stuetemperaturEt lag perovskit vises lasende grønt under kontinuerlig drift ved stuetemperatur. Forskning fra Kyushu University og Changchun Institute of Applied Chemistry, Det Kinesiske Videnskabsakademi, indikere
Kontinuerlig og stabil lasning opnået fra billige perovskitter ved stuetemperaturEt lag perovskit vises lasende grønt under kontinuerlig drift ved stuetemperatur. Forskning fra Kyushu University og Changchun Institute of Applied Chemistry, Det Kinesiske Videnskabsakademi, indikere -
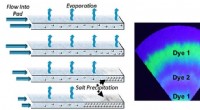 Papirbaseret enhed giver lavt strømforbrug, langsigtet metode til at analysere svedFordampningen af sved på papirpuder kunne bruges til væsketransport i wearables over lange perioder. Det resulterende tørre lag af kagede salte ville bevare en tidsstemplet registrering af biomarkør
Papirbaseret enhed giver lavt strømforbrug, langsigtet metode til at analysere svedFordampningen af sved på papirpuder kunne bruges til væsketransport i wearables over lange perioder. Det resulterende tørre lag af kagede salte ville bevare en tidsstemplet registrering af biomarkør -
 Kontrol af fremstilling af stabile aerogelerForfatterne og den nyudviklede porøse gel. Kredit:Kyoto University iCeMS Kyoto -universitetets forskere har udviklet en ny tilgang til at kontrollere fremstilling af bløde, porøse materialer, over
Kontrol af fremstilling af stabile aerogelerForfatterne og den nyudviklede porøse gel. Kredit:Kyoto University iCeMS Kyoto -universitetets forskere har udviklet en ny tilgang til at kontrollere fremstilling af bløde, porøse materialer, over -
 Brug af elektricitet til at skabe forbindelser til lægemidler, andre kemikalierKredit:CC0 Public Domain Hvad har krudt, penicillin og teflon til fælles? De var opfindelser, der tog verden med storm, men de blev alle skabt ved et fuldstændigt tilfælde. I en ny undersøgelse of
Brug af elektricitet til at skabe forbindelser til lægemidler, andre kemikalierKredit:CC0 Public Domain Hvad har krudt, penicillin og teflon til fælles? De var opfindelser, der tog verden med storm, men de blev alle skabt ved et fuldstændigt tilfælde. I en ny undersøgelse of
- Hvordan man bruger rødtsaft til at lave en PH Scale
- Forskere bryder forbindelsen mellem et kvantematerialespin og orbitale tilstande
- Californiens guvernør overvejer en-tunnel vandplan
- Hvad er 10 forskellige faste husholdningsstoffer?
- Forskere bruger sjældne jordarters metaller i legeringspulvere til at producere grønne, iøjnefald…
- Hastigheden af et objekt i en bestemt retning?


