Hvorfor vil natrium og kalium reagere eller ikke reagere på en binding med hinanden?
* Elektrostatisk frastødning: Både natrium og kalium er alkalimetaller, hvilket betyder, at de har en enkelt valenselektron og er meget elektropositive. Når de nærmer sig hinanden, afviser deres positivt ladede kerner hinanden.
* Lignende elektronegativitet: Natrium og kalium har meget ens elektronegativitetsværdier. Dette betyder, at de har en lignende tendens til at tiltrække elektroner. Som et resultat er der ingen signifikant forskel i deres elektrondelingsfunktioner, hvilket gør dannelsen af en kovalent obligation usandsynlig.
* Metallisk binding: Både natrium og kalium er metaller, og deres primære bindingsmekanisme er metallisk binding. Dette involverer et "hav" af delokaliserede elektroner, der holder metalatomerne sammen. De danner ikke stærke bånd med hinanden.
Kortfattet: Den elektrostatiske frastødelse mellem deres positivt ladede kerner og deres lignende elektronegativitetsværdier forhindrer natrium og kalium i at danne en stabil binding.
Sidste artikelEr natriumbisulfat og soda-ash det samme?
Næste artikelHvor mange mol ammoniumioner er i 4,50 mol NH4 2CO3?
 Varme artikler
Varme artikler
-
 Forskerhold øger klæbeevnen af silikone ved at bruge eksemplet med billerForskellige konfigurationer ændrer den klæbende effekt af silikonematerialet, hvis overflade har fået en svampelignende struktur. Vedhæftningen er bedst, når den er bøjet konkav (højre). Kredit:© Emre
Forskerhold øger klæbeevnen af silikone ved at bruge eksemplet med billerForskellige konfigurationer ændrer den klæbende effekt af silikonematerialet, hvis overflade har fået en svampelignende struktur. Vedhæftningen er bedst, når den er bøjet konkav (højre). Kredit:© Emre -
 Hvordan vitaminer, steroider og potentielle antivirale midler kan påvirke SARS-CoV-2Kredit:Pixabay/CC0 Public Domain Der er vidnesbyrd om, at D-vitamin – og muligvis K- og A-vitamin – kan hjælpe med at bekæmpe COVID-19. En ny undersøgelse fra University of Bristol offentliggjort
Hvordan vitaminer, steroider og potentielle antivirale midler kan påvirke SARS-CoV-2Kredit:Pixabay/CC0 Public Domain Der er vidnesbyrd om, at D-vitamin – og muligvis K- og A-vitamin – kan hjælpe med at bekæmpe COVID-19. En ny undersøgelse fra University of Bristol offentliggjort -
 Ny syntesestrategi fremskynder identifikation af enklere versioner af et naturproduktBaylor University professor og kemiker Daniel Romo, Ph.D., diskuterer forskning med ph.d.-kandidat Christian M. Chaheine, medforfatter på ny syntesestrategi. Undersøgelsen er publiceret i Naturkemi
Ny syntesestrategi fremskynder identifikation af enklere versioner af et naturproduktBaylor University professor og kemiker Daniel Romo, Ph.D., diskuterer forskning med ph.d.-kandidat Christian M. Chaheine, medforfatter på ny syntesestrategi. Undersøgelsen er publiceret i Naturkemi -
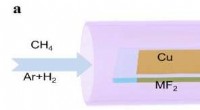 Fluor fremskynder todimensionel materialevækstSkematiske diagrammer over det eksperimentelle design til lokalt at introducere fluor til grafenvækst. Kredit:IBS Tilbage i 2004, fysikfællesskabet var lige begyndt at erkende eksistensen af vir
Fluor fremskynder todimensionel materialevækstSkematiske diagrammer over det eksperimentelle design til lokalt at introducere fluor til grafenvækst. Kredit:IBS Tilbage i 2004, fysikfællesskabet var lige begyndt at erkende eksistensen af vir
- Hvilken energi forvandles i et lejrbål?
- En ny løser til omtrentlig marginal kortslutning
- Brugereksperiment hos BESSY II—komplekse tesselleringer, ekstraordinære materialer
- Hvilken slags økosystem lever tigre i?
- Hvilket sammensat navn er RBCLO2?
- Hvordan udtrykker man det elektriske felt på grund af en punktladning i cylindriske koordinater?


