Solid CACL2 udfører ikke elektricitet forklarer, hvorfor det anses for at være en elektrolyt.?
* elektrolytter er stoffer, der udfører elektricitet, når de opløses i et opløsningsmiddel eller når de smeltes.
* solid cacl₂: I sin faste tilstand er calcium- og chloridioner tæt bundet i et krystallinsk gitter. Ionerne er ikke frie til at bevæge sig, hvilket forhindrer strømmen af elektrisk strøm.
* opløst eller smeltet cacl₂: Når cacl₂ opløses i vand eller smeltes, bryder de ioniske bindinger, og Ca²⁺- og Cl⁻ionen bliver fri til at bevæge sig. Disse mobile ioner kan derefter bære en elektrisk strøm.
Kortfattet:
* Solid cacl₂ er ikke En elektrolyt, fordi den ikke udfører elektricitet.
* Opløst eller smeltet cacl₂ er En elektrolyt, fordi de frie ioner kan udføre elektricitet.
Dette er grunden til, at CACL₂ bruges i forskellige applikationer, såsom afisning af veje og i batterielektrolytter, hvor dens evne til at udføre elektricitet i opløsning er afgørende.
 Varme artikler
Varme artikler
-
 Forbløffende grøn syntesemetode til højteknologiske farvestofferVed stuetemperatur er farvestoffet indigo fuldstændigt vandafvisende. En dråbe vand perler let af. Kredit:Vienna University of Technology Farvestoffer, der også er af stor interesse for organisk e
Forbløffende grøn syntesemetode til højteknologiske farvestofferVed stuetemperatur er farvestoffet indigo fuldstændigt vandafvisende. En dråbe vand perler let af. Kredit:Vienna University of Technology Farvestoffer, der også er af stor interesse for organisk e -
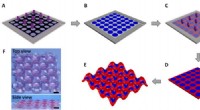 Periodisk mønstrede hydrogeler:en model for kooperativ deformationFotolitografisk mønster af gel og hævelse-induceret kooperativ deformation. (A) en forløberopløsning i reaktionscellen blev udsat for ultraviolet (UV) lysbestråling gennem en maske for at producere mø
Periodisk mønstrede hydrogeler:en model for kooperativ deformationFotolitografisk mønster af gel og hævelse-induceret kooperativ deformation. (A) en forløberopløsning i reaktionscellen blev udsat for ultraviolet (UV) lysbestråling gennem en maske for at producere mø -
 Molekyler omdanner synligt lys til ultraviolet lys med rekordeffektivitetEt nyudviklet molekylært system i glasrøret til højre opkonverterer effektivt synligt lys selv fra typiske LEDer til ultraviolet lys gennem triplet-triplet udslettelse. Udviklet af forskere ved Kyushu
Molekyler omdanner synligt lys til ultraviolet lys med rekordeffektivitetEt nyudviklet molekylært system i glasrøret til højre opkonverterer effektivt synligt lys selv fra typiske LEDer til ultraviolet lys gennem triplet-triplet udslettelse. Udviklet af forskere ved Kyushu -
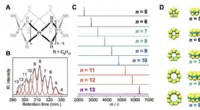 En forberedende reaktion ved hjælp af platinklynger med en encifret atomicitet realiseretFigur (A) viser kompleksernes kemiske struktur, (B) viser kromatogrammet for HPLC -adskillelsen med størrelsesekskluderingskolonner, (C) viser MALDI-TOF-massespektre for de isolerede platinkomplekser
En forberedende reaktion ved hjælp af platinklynger med en encifret atomicitet realiseretFigur (A) viser kompleksernes kemiske struktur, (B) viser kromatogrammet for HPLC -adskillelsen med størrelsesekskluderingskolonner, (C) viser MALDI-TOF-massespektre for de isolerede platinkomplekser
- Giv alle forskellige laboratorieudstyr og deres anvendelser?
- High-speed og on-silicium-chip graphene blackbody emittere
- Hvorfor afhænger de konstellationer, du ser, af breddegrad og tidsår?
- Hvordan finder man massen af opvarmet luft?
- Forskere hjælper med at sondere mørk energi ved at teste tyngdekraften
- Viser kort eller kloder de nøjagtige former?


