Er forholdet mellem atomer altid det samme i en forbindelse?
Her er hvorfor:
* Kemisk formel: Hver forbindelse har en specifik kemisk formel, der repræsenterer det nøjagtige forhold mellem atomer for hvert element, der er til stede i forbindelsen. For eksempel har vand (H₂O) altid to hydrogenatomer og et iltatom.
* Kemiske bindinger: Atomer binder sig sammen på specifikke måder at danne molekyler. Typen og antallet af bindinger, som et atom kan danne, bestemmes af dets elektroniske struktur. Dette betyder, at forholdet mellem atomer i en forbindelse dikteres af de specifikke kemiske bindinger, der dannes.
* Kemiske reaktioner: Kemiske reaktioner involverer omarrangement af atomer, men det samlede antal atomer i hvert element forbliver konstant. Dette betyder, at forholdet mellem atomer i produkterne fra en reaktion skal være det samme som forholdet mellem atomer i reaktanterne.
Eksempel:
Overvej den sammensatte kuldioxid (CO₂):
* Det indeholder altid et carbonatom og to iltatomer, uanset dets kilde eller hvordan det dannes.
* Forholdet mellem kulstof og iltatomer er altid 1:2.
Undtagelser:
Mens loven i bestemte proportioner gælder for de fleste forbindelser, er der nogle undtagelser:
* polymerer: Polymerer kan have variable kædelængder, hvilket fører til små variationer i forholdet mellem atomer.
* ikke-støkiometriske forbindelser: Dette er forbindelser, hvor forholdet mellem atomer ikke er et simpelt antal hele tal, ofte på grund af defekter i deres krystalstrukturer.
Imidlertid er disse undtagelser relativt sjældne, og loven i bestemte proportioner er stadig et grundlæggende princip i kemi.
Sidste artikelHvor mange atomer og elementer er der i brintperoxid?
Næste artikelGennemgår ingen kemisk ændring under en reaktion?
 Varme artikler
Varme artikler
-
 Biologisk materiale øger solcellens ydeevneCongcong Wu, forskningslektor ved Penn State, arbejder med materialer, der kan indsættes i næste generation af solceller for at forbedre deres effektivitet. Perovskite solceller er et område med inten
Biologisk materiale øger solcellens ydeevneCongcong Wu, forskningslektor ved Penn State, arbejder med materialer, der kan indsættes i næste generation af solceller for at forbedre deres effektivitet. Perovskite solceller er et område med inten -
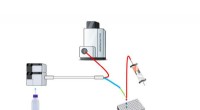 Nanofraktioneringsplatform med parallel massespecifikation til ID cytochrom CYP1A2-hæmmereGenerering af fase I metabolisk blanding af et lægemiddel efterfølges af kromatografisk adskillelse af metabolitterne. En split leder eluent til MS til identifikation af forbindelsen og til nanofrakti
Nanofraktioneringsplatform med parallel massespecifikation til ID cytochrom CYP1A2-hæmmereGenerering af fase I metabolisk blanding af et lægemiddel efterfølges af kromatografisk adskillelse af metabolitterne. En split leder eluent til MS til identifikation af forbindelsen og til nanofrakti -
 Selvemitterede overfladebølger i dynamisk brud af siliciumenkeltkrystalDynamisk revnefrontadfærd i steady-state (110) spaltning af de enkeltkrystallinske siliciumprøver under ren bøjning. (A) Morfologier af (110) spaltningsplanet (xy-planet) af de as-sawne prøver ved for
Selvemitterede overfladebølger i dynamisk brud af siliciumenkeltkrystalDynamisk revnefrontadfærd i steady-state (110) spaltning af de enkeltkrystallinske siliciumprøver under ren bøjning. (A) Morfologier af (110) spaltningsplanet (xy-planet) af de as-sawne prøver ved for -
 Billig vedvarende energi:Knækker den fotosynteseproces, der gør det muligt for planter at spalte v…Hvis mennesker kunne spalte vand ved hjælp af billige materialer som naturen gjorde, samfundet ville have en endeløs forsyning af billigt brintbrændstof til transport, uden kulstofemissioner. Kredit:J
Billig vedvarende energi:Knækker den fotosynteseproces, der gør det muligt for planter at spalte v…Hvis mennesker kunne spalte vand ved hjælp af billige materialer som naturen gjorde, samfundet ville have en endeløs forsyning af billigt brintbrændstof til transport, uden kulstofemissioner. Kredit:J
- Hvor meget vejer en mol jernatomer?
- USA opnåede et stort gennembrud for nuklear fusion. Her er grunden til, at magten stadig er årtier…
- Sådan konverteres fra mol pr. Liter til procent
- En vej til at undgå defekter under additiv fremstilling
- NASA-NOAA satellit finder cyklonen Hikaa ved Omans kyst
- Twitter advarer globale brugere om, at deres tweets overtræder pakistansk lov


