Hvordan finder du formlen for kobber 2 -fosfat?
1. Identificer ionerne
* kobber (ii): Dette fortæller os, at kobberionen har en +2 ladning (Cu²⁺).
* fosfat: Dette er den polyatomiske ion -po₄³⁻.
2. Bestem forholdet
* For at afbalancere ladningerne har du brug for tre kobber (II) -ioner (3 x +2 =+6) og to fosfationer (2 x -3 =-6).
3. Skriv formlen
Formlen for kobber (II) phosphat er cu₃ (po₄) ₂ .
Forklaring af formlen
* cu₃: Dette indikerer, at der er tre kobberatomer.
* (po₄) ₂: Dette indikerer, at der er to phosphatgrupper, der hver indeholder et phosphoratom og fire iltatomer.
Nøglepunkter
* romerske tal: Det romerske tal "II" i kobber (II) angiver dens oxidationstilstand, som er +2.
* polyatomiske ioner: Phosphat (Po₄³⁻) er en polyatomisk ion, hvilket betyder, at det er en gruppe af atomer, der fungerer som en enkelt enhed med et ladning.
* afbalanceringsafgifter: Kemiske formler skrives for at sikre, at den samlede ladning af forbindelsen er neutral.
Sidste artikelHvor brint kan gøres til en væske?
Næste artikelHvorfor binder nitrogen ikke mere end 4 andre atomer?
 Varme artikler
Varme artikler
-
 Brændstofaerosoler reducerer forurening af miljøetKredit:Tomsk Polytechnic University (TPU) En ressourceeffektiv teknologi til produktion af brændstofaerosoler er blevet udviklet ved Tomsk Polytechnic University. Udviklingen kan bruges til hurtig
Brændstofaerosoler reducerer forurening af miljøetKredit:Tomsk Polytechnic University (TPU) En ressourceeffektiv teknologi til produktion af brændstofaerosoler er blevet udviklet ved Tomsk Polytechnic University. Udviklingen kan bruges til hurtig -
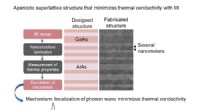 Minimering af termisk ledningsevne af krystallinsk materiale med optimal nanostrukturDen optimale nanostruktur designet med MI (aperiodisk supergitterstruktur) blev faktisk fremstillet, og den optimale ydeevne blev verificeret ved at vurdere dens varmeledningsevne. Figur:Den faktiske
Minimering af termisk ledningsevne af krystallinsk materiale med optimal nanostrukturDen optimale nanostruktur designet med MI (aperiodisk supergitterstruktur) blev faktisk fremstillet, og den optimale ydeevne blev verificeret ved at vurdere dens varmeledningsevne. Figur:Den faktiske -
 Undersøgelse af glasovergangsdynamik i flydende polymer ved hjælp af røntgenstrålerKredit:CC0 Public Domain Potentialet ved en røntgenspektroskopiteknik til at kaste lys over de mystiske fænomener, der opstår, når en væske nærmer sig en glaslignende tilstand, er blevet demonstre
Undersøgelse af glasovergangsdynamik i flydende polymer ved hjælp af røntgenstrålerKredit:CC0 Public Domain Potentialet ved en røntgenspektroskopiteknik til at kaste lys over de mystiske fænomener, der opstår, når en væske nærmer sig en glaslignende tilstand, er blevet demonstre -
 Molecular switch vil lette udviklingen af banebrydende elektro-optiske enhederEt forskerhold ved det tekniske universitet i München har udviklet molekylære nanoswitches, der kan skiftes mellem to strukturelt forskellige tilstande ved hjælp af en påført spænding. De kan tjene so
Molecular switch vil lette udviklingen af banebrydende elektro-optiske enhederEt forskerhold ved det tekniske universitet i München har udviklet molekylære nanoswitches, der kan skiftes mellem to strukturelt forskellige tilstande ved hjælp af en påført spænding. De kan tjene so
- Definition af primærforbruger
- Hvordan Canada kunne drage fordel af et CO2-budget
- Gamle mennesker forlod Afrika for at undslippe det tørre klima
- Hvad kaldes det, når du spreder et frø på marken tilfældigt?
- Kvantforvikling i kemiske reaktioner? Nu er der en måde at finde ud af det på
- At knække, hvordan liv opstod på Jorden, kan hjælpe med at afklare, hvor det ellers kunne eksiste…


