Kan molekyler med molekylære formler C4H10 og C4H10O være isomerer af hinanden hvorfor eller hvorfor ikke?
* isomerer er molekyler, der har den samme molekylære formel, men forskellige strukturelle arrangementer af atomer.
* molekylær formel Repræsenterer det samlede antal atomer for hvert element i et molekyle.
I dette tilfælde er de molekylære formler C4H10 og C4H10O forskellige. Den anden formel inkluderer et iltatom, som den første mangler. Derfor har disse molekyler forskellige sammensætninger og kan ikke være isomerer.
her er en yderligere forklaring:
* C4H10 Repræsenterer kulbrinter kaldet Butanes. Der er to isomerer af butan:n-butan (lige kæde) og isobutan (forgrenet kæde).
* C4H10O Repræsenterer en række forbindelser, herunder alkoholer (som butanol), ethere (som diethylether) og andre. Disse forbindelser har forskellige funktionelle grupper (som -OH -gruppen i alkoholer) og forskellige strukturelle arrangementer end Butanes.
Kort sagt, for at være isomerer, skal molekyler have den samme molekylære formel, men forskellige strukturelle arrangementer. C4H10 og C4H10O har forskellige molekylære formler, så de kan ikke være isomerer.
Sidste artikelHvilken slags fast er KCL?
Næste artikelHvor mange mol aluminiumhydroxid er 39,0 g?
 Varme artikler
Varme artikler
-
 Kemikere designer hurtigere produktionsproces for essentielle sukkerarterKredit:CC0 Public Domain Celler fra alle levende organismer er dækket af et tæt lag af meget komplekse kulhydrater. Disse kulhydrater, som også er kendt som glykaner, er væsentlige mediatorer af e
Kemikere designer hurtigere produktionsproces for essentielle sukkerarterKredit:CC0 Public Domain Celler fra alle levende organismer er dækket af et tæt lag af meget komplekse kulhydrater. Disse kulhydrater, som også er kendt som glykaner, er væsentlige mediatorer af e -
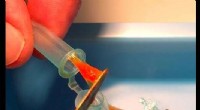 Sneglelim afslører ledetråde til at lave bedre medicinske klæbemidlerForskere studerer, hvordan sneglelim opnår sin stærke klæbeevne og fleksibilitet, indsigt, der kunne bruges til at skabe bedre medicinske klæbemidler. Kredit:Rebecca Falconer, Ithaca College Dusky
Sneglelim afslører ledetråde til at lave bedre medicinske klæbemidlerForskere studerer, hvordan sneglelim opnår sin stærke klæbeevne og fleksibilitet, indsigt, der kunne bruges til at skabe bedre medicinske klæbemidler. Kredit:Rebecca Falconer, Ithaca College Dusky -
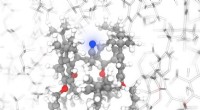 AI- og NMR-spektroskopi bestemmer atomernes konfiguration på rekordtidKredit:Michele Ceriotti / EPFL Mange lægemidler fremstilles i dag som faste stoffer i pulverform. Men for fuldt ud at forstå, hvordan de aktive ingredienser vil opføre sig en gang inde i kroppen,
AI- og NMR-spektroskopi bestemmer atomernes konfiguration på rekordtidKredit:Michele Ceriotti / EPFL Mange lægemidler fremstilles i dag som faste stoffer i pulverform. Men for fuldt ud at forstå, hvordan de aktive ingredienser vil opføre sig en gang inde i kroppen, -
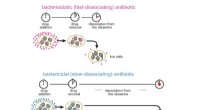 At lære antibiotika at være mere effektive dræbereForskning viser, at langvarig hæmning af proteinsyntese fører til celledød. Kredit:Proceedings of the National Academy of Sciences Forskning fra University of Illinois i Chicago tyder på bindingsv
At lære antibiotika at være mere effektive dræbereForskning viser, at langvarig hæmning af proteinsyntese fører til celledød. Kredit:Proceedings of the National Academy of Sciences Forskning fra University of Illinois i Chicago tyder på bindingsv
- Kan du lave dit eget hjemmelavede rumfartøj?
- Ser dybere ind i nanomaterialer:Nyt 3D-billedværktøj opnår den højeste opløsning endnu
- Hvad er definitionen af termodynamik?
- Hvordan globale COVID-19-pandemirestriktioner kaster lys over forholdet mellem transport og luftforu…
- Hvordan er det menneskelige genomprojekt relateret til genterapi?
- Hvilket slag beskriver den nuværende geologiske alder?


