Hvorfor er reaktionen mellem jod og acetone katalyseret?
mekanismen
1. Protonation af acetone: Reaktionen starter med protonationen af acetone ved en hydrogenion. Dette danner en enolat ion , som er en resonansstabiliseret anion.
2. nukleofil angreb: Enolationen er en stærk nukleofil og angriber jodmolekylet. Dette danner en iodoaceton Molekyle og iodidion (I-).
3. genprotonering: Iodoacetonmolekylet genprotoneres derefter ved et vandmolekyle, der regenererer acetonmolekylet.
Hvorfor er der behov for en katalysator?
* lav reaktionshastighed: Den direkte reaktion mellem jod og acetone er meget langsom, fordi acetone er en svag nukleofil.
* enolat iondannelse: Protoneringen af acetone danner enolationen, som er en meget stærkere nukleofil og let kan reagere med jod.
* ligevægtsskift: Tilsætningen af syre (H+) skifter ligevægt mod dannelsen af enolationen, hvilket øger reaktionens hastighed.
Kortfattet
Hydrogenionkatalysatoren fungerer som en proton donor og sænker aktiveringsenergien til reaktionen. Dette får reaktionen til at fortsætte meget hurtigere.
 Varme artikler
Varme artikler
-
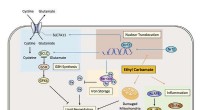 Forskere opdager mekanismen for ethylcarbamat-induceret toksicitet i fermenteret madKredit:Redox Biology Ethylcarbamat (EC) er et farligt stof, der naturligt produceres under gæringen af fødevarer og drikkevarer. Det er blevet kategoriseret som sandsynligvis kræftfremkaldende f
Forskere opdager mekanismen for ethylcarbamat-induceret toksicitet i fermenteret madKredit:Redox Biology Ethylcarbamat (EC) er et farligt stof, der naturligt produceres under gæringen af fødevarer og drikkevarer. Det er blevet kategoriseret som sandsynligvis kræftfremkaldende f -
 Forskere bruger nye teknologier for at se vand som aldrig førKredit:Pxhere Fra skabelsen af en enkelt dråbe til strømmen af en flod og verdens hydrologiske kredsløb – hvordan vand binder sammen, og til forskellige overflader, har vidtrækkende konsekvens
Forskere bruger nye teknologier for at se vand som aldrig førKredit:Pxhere Fra skabelsen af en enkelt dråbe til strømmen af en flod og verdens hydrologiske kredsløb – hvordan vand binder sammen, og til forskellige overflader, har vidtrækkende konsekvens -
 Vil fremtidens superbatterier være lavet af havvand?Kredit:CC0 Public Domain Vi kender alle de genopladelige og effektive lithium-ion (Li-ion) batterier, der sidder i vores smartphones, bærbare computere og også i elbiler. Desværre, lithium er en
Vil fremtidens superbatterier være lavet af havvand?Kredit:CC0 Public Domain Vi kender alle de genopladelige og effektive lithium-ion (Li-ion) batterier, der sidder i vores smartphones, bærbare computere og også i elbiler. Desværre, lithium er en -
 Styring af termisk ledningsevne af polymerer med lysUnder omgivelsesbetingelser eller synligt lys (venstre side), polymeren er krystallinsk og har en høj varmeledningsevne. Når den er udsat for ultraviolet (UV) lys (højre side), omdannes den til en væs
Styring af termisk ledningsevne af polymerer med lysUnder omgivelsesbetingelser eller synligt lys (venstre side), polymeren er krystallinsk og har en høj varmeledningsevne. Når den er udsat for ultraviolet (UV) lys (højre side), omdannes den til en væs
- Kan du nævne tre slags ændringer, der indikerer, at en kemisk reaktion har fundet sted?
- Landformer af græslandets biom
- Design af vandinfrastruktur til klimausikkerhed
- Hvilken type klima kendetegner den boreale nordlige skovbiome?
- Hvordan myggekontrollerende bakterier også kan forbedre insekternes frugtbarhed
- Hvilket af følgende er et polært molekyle F2 CO2 PF3 CF4 eller BF3?


