Når et atom af klor danner ionisk binding med klor?
* Elektronegativitet: Klor har en relativt høj elektronegativitet, hvilket betyder, at den har en stærk attraktion for elektroner.
* Lignende elektronegativitet: Når to kloratomer binder, er deres elektronegativiteter de samme. Dette betyder, at de har et lige træk på delte elektroner.
* kovalent binding: I stedet for at en elektron overføres (ionisk binding), deles elektronerne lige lige, hvilket resulterer i en kovalent binding . Dette skaber et diatomisk klormolekyle (CL₂).
Kortfattet: Kloratomer binder kovalent for at danne CL₂ -molekyler, ikke ionisk.
 Varme artikler
Varme artikler
-
 Videnskaben afslører hemmelighederne bag en mumies portræt(A) Portræt af en skægmand (Walters Art Museum #32.6), dateret c. 170-180 e.Kr. fra det romerske kejserlige Egypten; (B) Portrættet under ultraviolet lys. De lilla clavi på skuldrene ser pink-orange u
Videnskaben afslører hemmelighederne bag en mumies portræt(A) Portræt af en skægmand (Walters Art Museum #32.6), dateret c. 170-180 e.Kr. fra det romerske kejserlige Egypten; (B) Portrættet under ultraviolet lys. De lilla clavi på skuldrene ser pink-orange u -
 Din næste træstol kunne ankomme flad og derefter tørre til en 3D-formTræblæk trykt som et fladt rektangel er programmeret til at danne en kompleks form efter tørring og størkning. (Lineal er markeret i centimeter.). Kredit:Doron Kam Trægenstande fremstilles normalt
Din næste træstol kunne ankomme flad og derefter tørre til en 3D-formTræblæk trykt som et fladt rektangel er programmeret til at danne en kompleks form efter tørring og størkning. (Lineal er markeret i centimeter.). Kredit:Doron Kam Trægenstande fremstilles normalt -
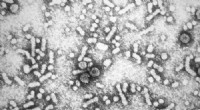 Forskere bruger supercomputer til at få indsigt i hepatitis BElektronmikroskopi af hepatitis B-virus. Kredit:Centers for Disease Control and Prevention Forskere ved University of Delaware, ved hjælp af supercomputeressourcer og samarbejde med forskere ved I
Forskere bruger supercomputer til at få indsigt i hepatitis BElektronmikroskopi af hepatitis B-virus. Kredit:Centers for Disease Control and Prevention Forskere ved University of Delaware, ved hjælp af supercomputeressourcer og samarbejde med forskere ved I -
 Kuldioxid-til-methanol-proces forbedret med katalysatorChunshan Song, venstre, og Xiao Jiang er to Penn State-forskere, der undersøger måder at bruge kuldioxid som råmateriale til at skabe brændstoffer og materialer. Song er direktør for EMS Energy Instit
Kuldioxid-til-methanol-proces forbedret med katalysatorChunshan Song, venstre, og Xiao Jiang er to Penn State-forskere, der undersøger måder at bruge kuldioxid som råmateriale til at skabe brændstoffer og materialer. Song er direktør for EMS Energy Instit
- Hvor mange volt elektricitet kan genereres, når du chokkerer nogen med statisk elektricitet?
- Hvad vil der ske med ledning, hvis det er bøjet?
- Hvilken vandmasse blev udforsket i år 1610?
- Hvilke former, når magma tvinger sig selv på tværs af klippelag?
- Identificer sundheds- og sikkerhedsfaktorer relateret til elektriske spændinger?
- Asteroid orus okkultation observeret for første gang nogensinde af eVscope


