Hvilket molekyle har den største delvis negative ladningschloridfluorbromi -jodcarbon?
* Elektronegativitet: Elektronegativitet er et atoms evne til at tiltrække elektroner i en binding. Jo højere elektronegativitet, jo stærkere er trækket på de delte elektroner.
* Periodiske tendenser: Elektronegativitet øges, når du bevæger dig over en periode (venstre til højre) og falder, når du bevæger dig ned ad en gruppe (top til bund) på den periodiske tabel.
Ser på listen:
* klor (CL), fluor (F), brom (BR), iod (I): Disse er alle halogener og er placeret i den samme gruppe. Jod er i bunden af gruppen, hvilket betyder, at den har den laveste elektronegativitet. Dette betyder, at i en binding vil jod have det svageste træk på delte elektroner, hvilket resulterer i den største delvis negative ladning.
* carbon (c): Carbon er ikke et halogen og har en lavere elektronegativitet end alle halogener.
Derfor vil jod have den største delvise negative ladning sammenlignet med de andre listede elementer.
Sidste artikelHvad er ligningen for ufuldstændig forbrænding af parafin?
Næste artikelHvor mange mol er der i 160 g brommolekyler?
 Varme artikler
Varme artikler
-
 Kemikere udvikler et nyt Washington Red-farvestof til bio-billeddannelseVisualisering af cellulært svovlbrinte ved hjælp af en Washington Red-baseret fluorescerende sensor. Kredit:WSU Forskere fra Washington State University har skabt et injicerbart farvestof, der bel
Kemikere udvikler et nyt Washington Red-farvestof til bio-billeddannelseVisualisering af cellulært svovlbrinte ved hjælp af en Washington Red-baseret fluorescerende sensor. Kredit:WSU Forskere fra Washington State University har skabt et injicerbart farvestof, der bel -
 Fremskridt i jagten på ukendte forbindelser i drikkevandKredit:CC0 Public Domain Et ukendt antal biprodukter dannes i drikkevandsbehandlingsprocessen, og forskere ved ikke, hvad mange af dem er. Imidlertid, ved hjælp af avanceret teknologi, forskere ve
Fremskridt i jagten på ukendte forbindelser i drikkevandKredit:CC0 Public Domain Et ukendt antal biprodukter dannes i drikkevandsbehandlingsprocessen, og forskere ved ikke, hvad mange af dem er. Imidlertid, ved hjælp af avanceret teknologi, forskere ve -
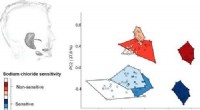 Spytproteiner kunne forklare, hvorfor nogle mennesker bruger for meget saltKredit:American Chemical Society Mange amerikanere indtager for meget salt. Nu i en undersøgelse, der vises i Journal of Agricultural and Food Chemistry , forskere rapporterer, at mennesker, der
Spytproteiner kunne forklare, hvorfor nogle mennesker bruger for meget saltKredit:American Chemical Society Mange amerikanere indtager for meget salt. Nu i en undersøgelse, der vises i Journal of Agricultural and Food Chemistry , forskere rapporterer, at mennesker, der -
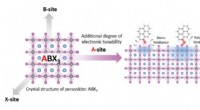 Ny måde at tænde for nanomaterialer til elektroniske applikationerSkematisk af perovskit materiale med organiske molekyler, der kan tilføje til dets elektroniske egenskaber. Kredit:Jingjing Xue og Rui Wang/UCLA Samueli School of Engineering UCLA materialeforsker
Ny måde at tænde for nanomaterialer til elektroniske applikationerSkematisk af perovskit materiale med organiske molekyler, der kan tilføje til dets elektroniske egenskaber. Kredit:Jingjing Xue og Rui Wang/UCLA Samueli School of Engineering UCLA materialeforsker
- Har nogen satellitter landet på Saturn?
- Kan jordalkalimetaller bruges i kvanteberegning?
- Hvordan er de forskellige typer energi ens og forskellige?
- Brug af byggematerialer til at overvåge for højt beriget uran
- Hvordan NQISRC'erne udnytter kvanterevolutionen
- Hvad er bølgelængden af en bølge med hastighed 345 ms og frekvens 600 Hz?


