Hvad er produktet af selvionisering SO2?
Her er hvorfor:
* Vands selvionisering: Vand (H2O) har en lille tendens til at donere en proton (H+) til et andet vandmolekyle, der danner hydroniumioner (H3O+) og hydroxidioner (OH-). Dette er repræsenteret af ligevægten:
`` `
2 H2O <=> H3O + + OH-
`` `
* SO2s natur: Svovldioxid er en kovalent forbindelse. Dens binding involverer deling af elektroner, og det danner ikke let ioner som vand gør. Mens SO2 kan reagere med vand til dannelse af svovlsyre (H2SO3), er dette en tydelig kemisk reaktion, ikke en selvioniseringsproces.
Sammenfattende har SO2 ikke et "produkt af selvionisering", fordi det ikke selvinioriseres på samme måde som vand.
 Varme artikler
Varme artikler
-
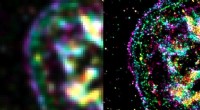 Kemikere gør cellulære kræfter synlige på molekylær skalaBilledet til venstre viser kraftaktiviteten af en celle ved en opløsning på omkring 250 nanometer. Billedet til højre viser, hvor meget klarere og skarpere billedet bliver med den opløsning på 25 na
Kemikere gør cellulære kræfter synlige på molekylær skalaBilledet til venstre viser kraftaktiviteten af en celle ved en opløsning på omkring 250 nanometer. Billedet til højre viser, hvor meget klarere og skarpere billedet bliver med den opløsning på 25 na -
 At bryde grænsen for kemiske forbindelserKredit:CC0 Public Domain Siden slutningen af det 19. århundrede, overgangsmetalcarbonyler har været en vigtig og velkendt klasse af forbindelser inden for koordinationskemi og organometallisk ke
At bryde grænsen for kemiske forbindelserKredit:CC0 Public Domain Siden slutningen af det 19. århundrede, overgangsmetalcarbonyler har været en vigtig og velkendt klasse af forbindelser inden for koordinationskemi og organometallisk ke -
 Avancerede polymerer hjælper med at strømline vandrensning, miljøsaneringProfessor Xiao Su, venstre, kandidatstuderende Stephen Cotty, centrum, og postdoc-forsker Kwiyong Kim har udviklet et energieffektivt apparat, der selektivt absorberer en meget giftig form for arsen i
Avancerede polymerer hjælper med at strømline vandrensning, miljøsaneringProfessor Xiao Su, venstre, kandidatstuderende Stephen Cotty, centrum, og postdoc-forsker Kwiyong Kim har udviklet et energieffektivt apparat, der selektivt absorberer en meget giftig form for arsen i -
 Let pincet kan bevæge sig, smelte, og spred mystiske biologiske isbjergeEksperimentel opstilling (a) Skematisk overgange observeret i nærvær af 0,2 M NaCl. Adsorberede GUVer gik ikke altid over til SLBer, og det er på disse strukturer, at domæner kan manipuleres. b Fluore
Let pincet kan bevæge sig, smelte, og spred mystiske biologiske isbjergeEksperimentel opstilling (a) Skematisk overgange observeret i nærvær af 0,2 M NaCl. Adsorberede GUVer gik ikke altid over til SLBer, og det er på disse strukturer, at domæner kan manipuleres. b Fluore
- Klimavenlig metalproduktion:Hvorfor er det svært?
- Hvordan et nyt radiofrekvenskontrolsystem forbedrer kvantecomputere
- Hvad er grundlæggende teori inden for videnskab?
- Lys-interagerende nanostrukturer producerer en bemærkelsesværdig frekvensfordoblingseffekt
- Hvilket ord om ti bogstaver beskriver, hvordan sagen opfører sig?
- Ændringer af dyrefoder kan levere mad til 1 milliard mennesker


