CH2CCHCH3 Karbonerne er nummereret fra en til fire venstre højre, hvad er molekylær geometri af carbon 3 -hybridisering 4 bindingsvinkler 2?
Molekylet:
Formel CH2CCHCH3 repræsenterer en Butene Molekyle (specifikt 1-buten). Sådan ser det ud:
`` `
H
|
H - C =C - C - H
| | |
H H CH3
1 2 3 4
`` `
carbon 3
* Hybridisering: Carbon 3 er forbundet til tre andre atomer (to hydrogener og en carbon). Dette betyder, at det har tre elektrondomæner, hvilket gør det SP2 hybridiseret .
* molekylær geometri: SP2 -hybridisering resulterer i en trigonal plan Geometri omkring kulstof 3. Dette betyder, at de tre atomer, der er forbundet til carbon 3, ligger i et plan med bindingsvinkler på ca. 120 grader.
Bond vinkler
* carbon 2: Dette kulstof er også SP2 hybridiseret på grund af dobbeltbindingen, hvilket resulterer i en trigonal plane geometri med bindingsvinkler på cirka 120 grader.
* carbon 4: Dette kulstof er SP3 -hybridiseret (fire enkeltbindinger), hvilket resulterer i en tetrahedral geometri med bindingsvinkler på ca. 109,5 grader.
Kortfattet:
* carbon 3: SP2 -hybridisering, trigonal plan geometri, bindingsvinkler ~ 120 grader
* carbon 2: SP2 -hybridisering, trigonal plan geometri, bindingsvinkler ~ 120 grader
* carbon 4: SP3 -hybridisering, tetrahedral geometri, bindingsvinkler ~ 109,5 grader
Sidste artikelHvor findes natrium, og hvordan det opnåede?
Næste artikelHvad er oxid atomnummer?
 Varme artikler
Varme artikler
-
 Diamanter i dine enheder:Giver kraft til næste generation af energilagringI en banebrydende undersøgelse, videnskabsmænd fra Japan bruger nanodiamanter til at konstruere superkondensatorer, der i vid udstrækning kan bruges som et mere effektivt alternativ til konventionelle
Diamanter i dine enheder:Giver kraft til næste generation af energilagringI en banebrydende undersøgelse, videnskabsmænd fra Japan bruger nanodiamanter til at konstruere superkondensatorer, der i vid udstrækning kan bruges som et mere effektivt alternativ til konventionelle -
 Hvordan påvirker strømning kræfter af ladede overflader/partikler og overfladeaktive stoffer i væ…Væskestrøm muliggør mere adsorption. Kredit:© 2020 American Chemical Society Du er på kontoret. Du har skrevet en rapport og trykket på Udskriv. Gå hen til printeren og hent den friske, inkjet-try
Hvordan påvirker strømning kræfter af ladede overflader/partikler og overfladeaktive stoffer i væ…Væskestrøm muliggør mere adsorption. Kredit:© 2020 American Chemical Society Du er på kontoret. Du har skrevet en rapport og trykket på Udskriv. Gå hen til printeren og hent den friske, inkjet-try -
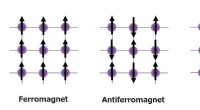 Forskere syntetiserer halvmetal uden magnetiseringSpinarrangement af magnetiske momenter i ferromagnetiske, antiferromagnetiske og ferrimagnetiske materialer. Kredit:Rie Umetsu En forskergruppe har med succes syntetiseret et halvmetal materiale og
Forskere syntetiserer halvmetal uden magnetiseringSpinarrangement af magnetiske momenter i ferromagnetiske, antiferromagnetiske og ferrimagnetiske materialer. Kredit:Rie Umetsu En forskergruppe har med succes syntetiseret et halvmetal materiale og -
 Ingeniører udvikler et programmerbart camouflerende materiale inspireret af blækspruttehudSepia apama (gigantisk australsk blæksprutte), der udtrykker sine papiller til camouflageformål. Kredit:Roger Hanlon Til blæksprutten og blæksprutten, Øjeblikkeligt at ændre deres hudfarve og møn
Ingeniører udvikler et programmerbart camouflerende materiale inspireret af blækspruttehudSepia apama (gigantisk australsk blæksprutte), der udtrykker sine papiller til camouflageformål. Kredit:Roger Hanlon Til blæksprutten og blæksprutten, Øjeblikkeligt at ændre deres hudfarve og møn
- Hvilke ioner skal du bruge for at bygge en ionforbindelse?
- Talegenkendelsesteknologi til flyveledere
- Har aluminiumssoda dåser titanium åbningsfaner?
- Hvorfor voldtægtsofre så ofte bliver overladt til at løse deres egne sager
- Analyse fremhæver fejl i USAs avancerede atomprogram
- Hvad sker der med ozonlaget i Stratoshere?


