Hvorfor har hydroxid en negativ ladning?
* Oxygen's stærke træk: Oxygen er meget elektronegativ, hvilket betyder, at det har en stærk attraktion for elektroner. I en hydroxidion (OH-) trækker iltatomet de delte elektroner i den kovalente binding med brint tættere på sig selv.
* ujævn deling: Denne ujævne deling af elektroner skaber en delvis negativ ladning på iltatomet og en delvis positiv ladning på brintatomet.
* det ensomme par: Oxygen har også to ensomme par elektroner, der ikke er involveret i binding. Disse ensomme par bidrager yderligere til den negative ladning på iltatomet.
* samlet afgift: Den kombinerede virkning af ilts elektronegativitet og de ensomme par giver hydroxidionen et netto negativt ladning.
i enklere termer: Oxygenatomet i hydroxid er som en magnet til elektroner, hvilket gør hele molekylet "elektronrig" og således lades negativt.
 Varme artikler
Varme artikler
-
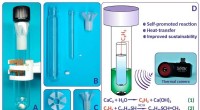 Kemikere opfinder et effektivt termisk kamera for at reducere omkostningerne til kemisk forskningReaktionsopsætningen ved hjælp af den udviklede rør-i-rør-reaktor:(A)—reaktoren klar til brug; (B)—den adskilte reaktor; (C)-nylonforing; (D)—termisk kamera og skemaet for rør-i-rør-reaktor og to trin
Kemikere opfinder et effektivt termisk kamera for at reducere omkostningerne til kemisk forskningReaktionsopsætningen ved hjælp af den udviklede rør-i-rør-reaktor:(A)—reaktoren klar til brug; (B)—den adskilte reaktor; (C)-nylonforing; (D)—termisk kamera og skemaet for rør-i-rør-reaktor og to trin -
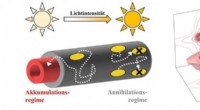 Energiflow i nanoområdetKredit:Billeder:Björn Kriete (v.) / Stefan Mueller (r.) Planter og bakterier kan fange sollysets energi med lys-høstende antenner og overføre den til et reaktionscenter. At transportere energi eff
Energiflow i nanoområdetKredit:Billeder:Björn Kriete (v.) / Stefan Mueller (r.) Planter og bakterier kan fange sollysets energi med lys-høstende antenner og overføre den til et reaktionscenter. At transportere energi eff -
 Overvejer duften af vinKredit:CC0 Public Domain En god vin har en ideel balance af ingredienser. For meget eller for lidt af en komponent kan betyde forskellen mellem en vin med en sød og frugtagtig aroma og en, der duf
Overvejer duften af vinKredit:CC0 Public Domain En god vin har en ideel balance af ingredienser. For meget eller for lidt af en komponent kan betyde forskellen mellem en vin med en sød og frugtagtig aroma og en, der duf -
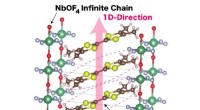 Forskere opdager ny organisk lederKrystalstruktur af en-dimensionel ladningsoverføringssalt med en uendelig anionkæde (TMTTF) (NbOF 4 ) Kredit:NINS/IMS Salte er langt mere komplicerede end fødevarekrydderiet - de kan endda funge
Forskere opdager ny organisk lederKrystalstruktur af en-dimensionel ladningsoverføringssalt med en uendelig anionkæde (TMTTF) (NbOF 4 ) Kredit:NINS/IMS Salte er langt mere komplicerede end fødevarekrydderiet - de kan endda funge
- En blanding af gasser indeholder 0,25 mol iltgas 0,75 nitrogen og 1,50 kuldioxid ved STP molfraktion…
- Af de otte D-aldohexoser, som er mest udbredt i den biologiske verden?
- Neutronstjernefusion bekræfter årtiers forudsigelser
- Sådan genaktiveres en desiccant
- Er salt lavet af to eller flere mineraler?
- Hvis forskydningen falder, er hastigheden?


