Brug partikelmodeller til at forklare, hvorfor væsker og gasser tager formen på deres containere?
partikelmodeller og formen på væsker og gasser
Partikelmodellen hjælper os med at forstå stoffets opførsel, herunder hvorfor væsker og gasser tager formen på deres containere.
1. Væsker:
* Partikelarrangement: Flydende partikler er tæt sammen, men kan bevæge sig rundt i hinanden. De har et fast volumen, hvilket betyder, at de optager et specifikt rum, men ingen fast form.
* Partikelbevægelse: Flydende partikler bevæger sig konstant og kolliderer, men de har ikke nok energi til at bryde fri fra hinanden som gaspartikler.
* form: Fordi partiklerne kan bevæge sig forbi hinanden, vil de flyde for at fylde formen på deres beholder. Derfor kan du hælde en væske i forskellige formede containere, og det vil tage formen på den nye beholder.
2. Gasser:
* Partikelarrangement: Gaspartikler er langt fra hinanden og bevæger sig frit i alle retninger. De har ingen fast volumen eller form.
* Partikelbevægelse: Gaspartikler bevæger sig meget hurtigt og kolliderer ofte med hinanden og væggene i deres beholder.
* form: Fordi partiklerne har så meget energi og spredes langt fra hinanden, vil de udfylde den beholder, de er i. Dette er grunden til, at gas udvides til at fylde hele volumenet af en beholder, uanset dens form.
her er en simpel analogi:
Forestil dig en kasse med kugler (der repræsenterer flydende partikler) og en gruppe hoppekugler (der repræsenterer gaspartikler).
* marmor: De vil forblive i kassen og tage formen på kassens bund, men hvis du hælder dem i en anden formet beholder, vil de påtage sig den nye form.
* hoppekugler: De vil hoppe rundt i kassen, sprede sig og slå siderne og toppen og påtage sig formen af hele kassen.
Kortfattet:
* væsker Har et fast volumen, men tag formen på deres beholder, fordi deres partikler er tæt på hinanden, men kan bevæge sig rundt om hinanden.
* Gasser Har ingen fast volumen eller form, fordi deres partikler er langt fra hinanden og bevæger sig frit, og udvides til at fylde den beholder, de er i.
Sidste artikelHvad er partiklerne, der udgør et atom?
Næste artikelHvordan ændrer partikler sig, som de angiver fra fast til væske?
 Varme artikler
Varme artikler
-
 Forskere bruger supercomputer til at få indsigt i hepatitis BElektronmikroskopi af hepatitis B-virus. Kredit:Centers for Disease Control and Prevention Forskere ved University of Delaware, ved hjælp af supercomputeressourcer og samarbejde med forskere ved I
Forskere bruger supercomputer til at få indsigt i hepatitis BElektronmikroskopi af hepatitis B-virus. Kredit:Centers for Disease Control and Prevention Forskere ved University of Delaware, ved hjælp af supercomputeressourcer og samarbejde med forskere ved I -
 Analyse giver fingerpeg om kemisk sammensætning, naturlig lagring af 100 år gammelt ølFor nylig opdagede øl fra første verdenskrig kunne hjælpe forskere med bedre at forstå de ældningsprocesser, der er involveret i brygning. Kredit:Brewing Institute, Prag Gemt væk og længe glemt, e
Analyse giver fingerpeg om kemisk sammensætning, naturlig lagring af 100 år gammelt ølFor nylig opdagede øl fra første verdenskrig kunne hjælpe forskere med bedre at forstå de ældningsprocesser, der er involveret i brygning. Kredit:Brewing Institute, Prag Gemt væk og længe glemt, e -
 Isolerende mursten med mikroskopiske boblerFor at opnå de samme isoleringsværdier som en 165 mm tyk væg af aerobricks, en mur af perlitsten skal være 263 mm tyk — og en mur af ikke-isolerende mursten skal være mere end en meter. Kredit:Empa
Isolerende mursten med mikroskopiske boblerFor at opnå de samme isoleringsværdier som en 165 mm tyk væg af aerobricks, en mur af perlitsten skal være 263 mm tyk — og en mur af ikke-isolerende mursten skal være mere end en meter. Kredit:Empa -
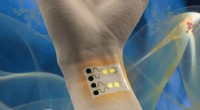 En bærbar gassensor til sundheds- og miljøovervågningEn bærbar gassensor kan overvåge miljømæssige og medicinske forhold. Kredit:Cheng Lab/Penn State En meget følsom, Bærbar gassensor til miljø- og sundhedsovervågning kan snart blive kommercielt til
En bærbar gassensor til sundheds- og miljøovervågningEn bærbar gassensor kan overvåge miljømæssige og medicinske forhold. Kredit:Cheng Lab/Penn State En meget følsom, Bærbar gassensor til miljø- og sundhedsovervågning kan snart blive kommercielt til
- Er der nogen stjerner i rummet?
- Hvad er puriner og pyrimidiner?
- Hvilket beskriver bedst organismer i den prækambriske æra?
- Hvem er et fysikprincip?
- Hvor mange ækvivalente fly 111 er der i en orthorhombisk krystal?
- En skadefri måde at måle sundheden for næste generations batterier til elektriske køretøjer


