Hvordan påvirker tilføjelse af varme molekylær bevægelse?
1. Øget translationel bevægelse: Molekyler bevæger sig hurtigere rundt, hvilket øger deres hastighed og ændrer deres position oftere. Dette er især tydeligt i gasser, hvor molekyler er fri til at bevæge sig i alle retninger.
2. Øget vibrationsbevægelse: Molekyler vibrerer hurtigere, hvilket fører til større amplitude i deres svingninger. Dette er vigtigt for faste stoffer og væsker, hvor molekyler er mere tæt bundet.
3. Øget rotationsbevægelse: Molekyler roterer hurtigere rundt om deres akser, hvilket øger deres vinkelhastighed. Dette er også betydningsfuldt for væsker og gasser, hvor molekyler har mere frihed til at rotere.
Effekter af øget molekylær bevægelse:
* Forøget temperatur: Den gennemsnitlige kinetiske energi af molekyler er direkte proportional med temperaturen. Når molekyler bevæger sig hurtigere, stiger stoffets temperatur.
* udvidelse: Generelt udvides stoffer, når de opvarmes på grund af den øgede afstand mellem molekyler forårsaget af deres hurtigere bevægelse.
* Ændringer i tilstand: Opvarmning kan få et stof til at ændre tilstand fra fast stof til væske (smeltning) eller fra væske til gas (kogning). Dette skyldes den øgede molekylære bevægelse, der overvinder kræfterne, der holder molekylerne sammen.
* øgede reaktionshastigheder: Hurtigere molekylær bevægelse fører til hyppigere kollisioner, hvilket øger sandsynligheden for kemiske reaktioner.
* Øget entropi: Entropi er et mål for forstyrrelse. Hurtigere molekylær bevægelse fører til en mere forstyrret tilstand, stigende entropi.
I resumé øger tilsætning af varme den kinetiske energi af molekyler, hvilket får dem til at bevæge sig hurtigere og mere kraftigt. Dette fører til flere effekter, herunder øget temperatur, ekspansion, ændringer i tilstand, øgede reaktionshastigheder og øget entropi.
 Varme artikler
Varme artikler
-
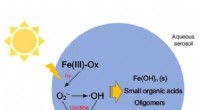 Virkninger af Fenton-lignende reaktioner af ferroloxalat på atmosfæriske oxidationsprocesser og st…Methacrolein reagerer med superoxidradikaler frembragt ved en Fenton-lignende reaktion. Dette påvirker atmosfærisk strålingsforcerende kraft på grund af dannelsen af uopløseligt jernhydroxid. Kredit
Virkninger af Fenton-lignende reaktioner af ferroloxalat på atmosfæriske oxidationsprocesser og st…Methacrolein reagerer med superoxidradikaler frembragt ved en Fenton-lignende reaktion. Dette påvirker atmosfærisk strålingsforcerende kraft på grund af dannelsen af uopløseligt jernhydroxid. Kredit -
 Krystallisering blev krystalklarKorrelation mellem cryo-transmission elektronmikroskop (TEM) billeder og krystalstrukturen. a) TEM -billede, der viser tre kolliderende klynger. Skalaen er 10 nm. b) Relative positioner af molekyler a
Krystallisering blev krystalklarKorrelation mellem cryo-transmission elektronmikroskop (TEM) billeder og krystalstrukturen. a) TEM -billede, der viser tre kolliderende klynger. Skalaen er 10 nm. b) Relative positioner af molekyler a -
 Formskiftende organiske krystaller bruger hukommelse til at forbedre plastikelektronikIllinois kemi og biomolekylær ingeniørprofessor Ying Diao, ret, og kandidatstuderende Hyunjoong Chung er en del af et team, der har identificeret en mekanisme, der udløser form-hukommelse i organiske
Formskiftende organiske krystaller bruger hukommelse til at forbedre plastikelektronikIllinois kemi og biomolekylær ingeniørprofessor Ying Diao, ret, og kandidatstuderende Hyunjoong Chung er en del af et team, der har identificeret en mekanisme, der udløser form-hukommelse i organiske -
 Klikreaktion for levende systemer:Bioortogonal hydroaminering af aktiverede lineære alkynerKredit:CC0 Public Domain At øge vores forståelse af cellulære processer kræver information om de involverede typer biomolekyler, deres placeringer, og deres interaktioner. Dette kræver, at molekyl
Klikreaktion for levende systemer:Bioortogonal hydroaminering af aktiverede lineære alkynerKredit:CC0 Public Domain At øge vores forståelse af cellulære processer kræver information om de involverede typer biomolekyler, deres placeringer, og deres interaktioner. Dette kræver, at molekyl
- Enzymcocktail udviklet i Brasilien driver produktionen af anden generations ethanol
- Højere opløsning i havmodeller:Er det det værd?
- Hvad er den videnskabelige definition for skorpe?
- Hvad er navnet på fysikkoncept, der anvendes i fly til, kan flyve?
- Forskere undersøger, hvordan en celles proteinfremstillingsfabrikker er samlet
- Hvad er accelerationen på grund af tyngdekraften, hvis et objekt falder ned fra en højde på 25 m?…


