Hvordan ændres hastigheden af molekyler en gas, når de opvarmes?
* kinetisk energi: Temperaturen på en gas er direkte relateret til den gennemsnitlige kinetiske energi for dens molekyler. Kinetisk energi er bevægelsesenergien.
* Varmeoverførsel: Når du tilsætter varme til en gas, overfører du energi til dens molekyler.
* Øget bevægelse: Denne tilsatte energi får molekylerne til at bevæge sig hurtigere, hvilket resulterer i en højere gennemsnitlig hastighed.
Tænk på det sådan: Forestil dig molekylerne af en gas som små kugler, der hopper rundt i en beholder. Når du opvarmer beholderen, giver du kuglerne mere energi. Dette får dem til at hoppe mere kraftigt omkring, hvilket fører til en højere hastighed.
Vigtig note: Hastigheden af individuelle molekyler i en gas ændrer sig konstant på grund af kollisioner. Imidlertid gennemsnitlig hastighed af molekylerne øges, når temperaturen stiger.
 Varme artikler
Varme artikler
-
 Eksperimentel vaccine sløver den dødeligste af syntetiske opioiderPotentielt dødelige doser af fentanyl og carfentanil er en brøkdel af dødelige mængder heroin, hvilket har udløst en alarmerende stigning i overdosisdødsfald. Kredit:U.S. Attorneys Office Da opioi
Eksperimentel vaccine sløver den dødeligste af syntetiske opioiderPotentielt dødelige doser af fentanyl og carfentanil er en brøkdel af dødelige mængder heroin, hvilket har udløst en alarmerende stigning i overdosisdødsfald. Kredit:U.S. Attorneys Office Da opioi -
 Forskere udvikler 3D-trykte biomaterialer, der nedbrydes efter behovBrune forskere har fundet en måde at 3D-udskrive indviklede midlertidige mikrostrukturer, der kan nedbrydes efter behov ved hjælp af en biokompatibel kemisk trigger. Teknikken kunne være nyttig kunne
Forskere udvikler 3D-trykte biomaterialer, der nedbrydes efter behovBrune forskere har fundet en måde at 3D-udskrive indviklede midlertidige mikrostrukturer, der kan nedbrydes efter behov ved hjælp af en biokompatibel kemisk trigger. Teknikken kunne være nyttig kunne -
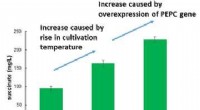 Verdens mest effektive produktion af succinat fra kuldioxidFigur 1:Øgede mængder succinat produceres baseret på overekspression af PEPC -gener og forhøjelse af dyrkningstemperaturen. Kredit:Kobe University Succinat bruges i vid udstrækning som en rå ingre
Verdens mest effektive produktion af succinat fra kuldioxidFigur 1:Øgede mængder succinat produceres baseret på overekspression af PEPC -gener og forhøjelse af dyrkningstemperaturen. Kredit:Kobe University Succinat bruges i vid udstrækning som en rå ingre -
 Ozon nedbryder THC aflejret på overflader fra tredjehånds cannabisrøgKredit:CC0 Public Domain Anden og tredjehånds tobaksrøg har fået masser af opmærksomhed, men meget mindre er kendt om de forbindelser, der aflejres på overflader fra cannabisrøg. Nu, forskere, der
Ozon nedbryder THC aflejret på overflader fra tredjehånds cannabisrøgKredit:CC0 Public Domain Anden og tredjehånds tobaksrøg har fået masser af opmærksomhed, men meget mindre er kendt om de forbindelser, der aflejres på overflader fra cannabisrøg. Nu, forskere, der
- Forvandles væske til en gas, når neon og argon opvarmes?
- Er genindførelse af grizzlybjørn 'en dødsdom' eller genskabelse af naturen? Idahos kommentarer er…
- Verdens mest kraftfulde magnet klar til afsendelse
- Hvad er et opgrænset bjerg?
- Utrahurtig magnetisme:Elektron-fonon-interaktioner undersøgt på BESSY II
- Forskere tager et skridt fremad i at forstå, hvordan man tackler kroniske infektioner med cystisk f…


