Når faste og flydende faser er i ligevægt, hvilken fase eller indeholder den større mængde energi?
* Intermolekylære kræfter: Molekyler i en væske har svagere intermolekylære kræfter (som hydrogenbindinger, dipol-dipolinteraktioner eller London-spredningskræfter) sammenlignet med molekyler i et fast stof. Dette betyder, at de har mere frihed til at bevæge sig rundt.
* kinetisk energi: De svagere kræfter i væsker tillader molekyler at have højere kinetisk energi (bevægelsesenergi). Dette betyder, at de vibrerer, roterer og oversætter lettere end molekyler i et fast stof.
* Fusionsvarme: For at ændre et fast stof til en væske skal du tilføje energi (varme) for at bryde de stærkere intermolekylære kræfter, der holder det faste stof sammen. Denne energi absorberes af stoffet og bliver en del af dets indre energi.
Tænk på det på denne måde:
Forestil dig en gruppe mennesker, der hylder tæt sammen i et koldt rum (solid tilstand). De holder alle fast på hinanden og bevæger sig knap. Forestil dig nu, at rummet varmer op (tilføjer varmeenergi). Folket begynder at bevæge sig mere, slippe fri fra nogle af deres stramme hold, og de er nu mere spredt (Liquid State). De har mere energi nu, hvilket giver mulighed for større bevægelse.
ligevægt:
Når en fast og væske er i ligevægt, betyder det, at hastigheden af smeltning (fast til væske) er lig med frysningshastigheden (væske til fast). På dette tidspunkt er energiindholdet i væsken og faste faser det samme, men de flydende molekyler har en større * fordeling * af energi på grund af deres svagere kræfter og øget mobilitet.
 Varme artikler
Varme artikler
-
 En venligere måde at håndtere nitratforurening påKredit:CC0 Public Domain At lære af naturen, forskere fra Center for Sustainable Resource Science i Japan og Korean Basic Science Institute (KBSI) har fundet en katalysator, der effektivt omdanner
En venligere måde at håndtere nitratforurening påKredit:CC0 Public Domain At lære af naturen, forskere fra Center for Sustainable Resource Science i Japan og Korean Basic Science Institute (KBSI) har fundet en katalysator, der effektivt omdanner -
 DNA-origami overskrider vigtige tærsklerI et første skridt danner forskere ved det tekniske universitet i München V-formede byggesten ved hjælp af DNA-origami-teknikker. Bestemt af åbningsvinklen samles et defineret antal byggesten selv i e
DNA-origami overskrider vigtige tærsklerI et første skridt danner forskere ved det tekniske universitet i München V-formede byggesten ved hjælp af DNA-origami-teknikker. Bestemt af åbningsvinklen samles et defineret antal byggesten selv i e -
 Superhurtig indsigt i mobilbegivenhederFrankfurt-forskere fulgte bevægelserne af dette lille molekyle - kun to tusindedele af tykkelsen af et stykke papir. RNA-aptameren ændrer sin struktur, når den binder hypoxanthin. De grønne nukleoba
Superhurtig indsigt i mobilbegivenhederFrankfurt-forskere fulgte bevægelserne af dette lille molekyle - kun to tusindedele af tykkelsen af et stykke papir. RNA-aptameren ændrer sin struktur, når den binder hypoxanthin. De grønne nukleoba -
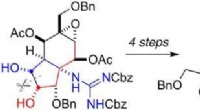 Fremstilling af pufferfisktoksin i en kolbeKredit:Angewandte Chemie I Japan, puffer fisk betragtes som en delikatesse, men kildren til smagsløgene kommer med en kildren til nerverne:fugu indeholder tetrodotoxin, et stærkt nervegift. I lave
Fremstilling af pufferfisktoksin i en kolbeKredit:Angewandte Chemie I Japan, puffer fisk betragtes som en delikatesse, men kildren til smagsløgene kommer med en kildren til nerverne:fugu indeholder tetrodotoxin, et stærkt nervegift. I lave


