Hvad er elektronkonfigurationen af fosfor?
1S² 2S² 2p⁶ 3S² 3p³
Her er en sammenbrud:
* 1S²: Det første energiniveau (n =1) har to elektroner i underskalet 'S'.
* 2s²: Det andet energiniveau (n =2) har to elektroner i underskalet 'S'.
* 2p⁶: Det andet energiniveau (n =2) har seks elektroner i underskalet 'P'.
* 3S²: Det tredje energiniveau (n =3) har to elektroner i underskalet 'S'.
* 3p³: Det tredje energiniveau (n =3) har tre elektroner i underskalet 'P'.
Vigtig note: Dette er jordtilstandens elektronkonfiguration. Fosfor kan også eksistere i ophidsede tilstande, hvor elektroner optager højere energiniveau.
Sidste artikelHvad er elektronkonfigurationen af ND?
Næste artikelHvad er en overførsel af molekyler, der støder på hinanden, der kaldes?
 Varme artikler
Varme artikler
-
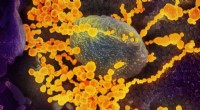 Forskere viser, at selvsteriliserende polymerer virker mod SARS-CoV-2Dette scanningselektronmikroskopbillede viser SARS-CoV-2 (runde guldobjekter), der dukker op fra overfladen af celler dyrket i laboratoriet. Kredit:NIAID-RML Forskere fra North Carolina State Un
Forskere viser, at selvsteriliserende polymerer virker mod SARS-CoV-2Dette scanningselektronmikroskopbillede viser SARS-CoV-2 (runde guldobjekter), der dukker op fra overfladen af celler dyrket i laboratoriet. Kredit:NIAID-RML Forskere fra North Carolina State Un -
 Ny tilgang til maskinlæring er bedre til at se enzymatiske metaller i proteinerJoanna Slusky, lektor i molekylær biovidenskab og beregningsbiologi ved University of Kansas, leder laboratoriet, hvor maskinlæring forbedrede præcisionen ved at identificere enzymatiske og ikke-enzym
Ny tilgang til maskinlæring er bedre til at se enzymatiske metaller i proteinerJoanna Slusky, lektor i molekylær biovidenskab og beregningsbiologi ved University of Kansas, leder laboratoriet, hvor maskinlæring forbedrede præcisionen ved at identificere enzymatiske og ikke-enzym -
 Ny beregningsmetode til screening identificerer potentielle faststofelektrolytterKredit:Nationalt Center for Kompetence i Forskning (NCCR) MARVEL Udskiftning af de flygtige og brandfarlige væsker eller polymerelektrolytter, der nu bruges i lithium-ion-batterier, med uorganiske
Ny beregningsmetode til screening identificerer potentielle faststofelektrolytterKredit:Nationalt Center for Kompetence i Forskning (NCCR) MARVEL Udskiftning af de flygtige og brandfarlige væsker eller polymerelektrolytter, der nu bruges i lithium-ion-batterier, med uorganiske -
 Masseproduktion af individualiserede produkterRobot-assisteret inkjet print på 3D overflader hos Fraunhofer ENAS. Kredit:Biermann&Jung Hvordan kan masseproduktionsmetoder anvendes på individualiserede produkter? Et svar er at bruge en kombina
Masseproduktion af individualiserede produkterRobot-assisteret inkjet print på 3D overflader hos Fraunhofer ENAS. Kredit:Biermann&Jung Hvordan kan masseproduktionsmetoder anvendes på individualiserede produkter? Et svar er at bruge en kombina
- Hvad er meningen med Hebibore?
- Hvad er jalousi? Hvordan adskiller jalousi sig fra misundelse?
- Ny teknologi konverterer plastaffald til jetbrændstof på en time
- Hvordan påvirkes centripetalkraften af masse og radius?
- Undersøgelse finder, at mere stabile ure kunne måle kvantefænomener, herunder tilstedeværelsen a…
- Molekylærbiologi:Er hurtigt prolifererende celler epigenetisk formbare?


