Hvad er tilstanden af stof, hvor molekyler er tættest sammen?
Her er hvorfor:
* faste stoffer Har en fast form og volumen, fordi deres molekyler er tæt pakket i et regelmæssigt, gentagne arrangement kaldet en krystalgitter. Denne nærhed og stærke tiltrækning mellem molekyler gør faste stoffer stive og ukomprimerbare.
* væsker har et fast volumen, men tag formen på deres beholder. Molekylerne er tættere sammen end i en gas, men de har mere frihed til at bevæge sig rundt end i et fast stof.
* Gasser Har ingen fast form eller volumen. Deres molekyler er langt fra hinanden og bevæger sig frit og kolliderer med hinanden og væggene i deres beholder.
Så selvom væsker har molekyler tættere sammen end gasser, har faste stoffer den nærmeste pakning og stærkeste intermolekylære kræfter.
 Varme artikler
Varme artikler
-
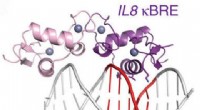 Duel af de inflammatoriske masterregulatorer – indsigt til lægemiddelopdagelseFigur:Diagram over glukokortikoidreceptoren, der binder et NF-kappaB-sted. Kredit:Hudson et al. Naturkommunikation (2018). Anti-inflammatoriske lægemidler såsom dexamethason kan have skadelige biv
Duel af de inflammatoriske masterregulatorer – indsigt til lægemiddelopdagelseFigur:Diagram over glukokortikoidreceptoren, der binder et NF-kappaB-sted. Kredit:Hudson et al. Naturkommunikation (2018). Anti-inflammatoriske lægemidler såsom dexamethason kan have skadelige biv -
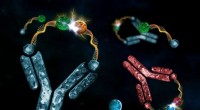 Sådan bruges antistoffer til at kontrollere kemiske reaktionerKunstnerisk fremstilling af to antistoffer, der udløser to kemiske reaktioner. Kredit:Oscar Melendre Hoyos I en samarbejdsindsats har en gruppe internationale forskere for nylig demonstreret en må
Sådan bruges antistoffer til at kontrollere kemiske reaktionerKunstnerisk fremstilling af to antistoffer, der udløser to kemiske reaktioner. Kredit:Oscar Melendre Hoyos I en samarbejdsindsats har en gruppe internationale forskere for nylig demonstreret en må -
 Naturlig blå madfarve får et miljøvenligt produktionsløftKredit:Pixabay/CC0 Public Domain Forskere har udviklet en miljøvenlig måde at øge produktionen og varmestabiliteten af en naturlig blå farve. Brugt i alt fra Smarties til gin, den blå farve, ke
Naturlig blå madfarve får et miljøvenligt produktionsløftKredit:Pixabay/CC0 Public Domain Forskere har udviklet en miljøvenlig måde at øge produktionen og varmestabiliteten af en naturlig blå farve. Brugt i alt fra Smarties til gin, den blå farve, ke -
 Brug af magneter til at kontrollere kemiske reaktioner, der målretter frigivelse af medicin inde i …E- og S-type superparamagnetiske nanopartikler, der bærer enzymet og substratet. en, b, Kryotransmission elektronmikroskopi (cryo-TEM) billede (a) og skematisk (b), der forklarer begrebet magnetfelt-u
Brug af magneter til at kontrollere kemiske reaktioner, der målretter frigivelse af medicin inde i …E- og S-type superparamagnetiske nanopartikler, der bærer enzymet og substratet. en, b, Kryotransmission elektronmikroskopi (cryo-TEM) billede (a) og skematisk (b), der forklarer begrebet magnetfelt-u
- Hvad er myten om Callisto?
- Forskere afslører mysteriet om van der Waals-magneter, et materiale til fremtidige halvledere
- Hvordan man opbygger et team af 'passende skeptiske' regnskabsrevisorer
- Fluorescerende jungle fitnesscentre lavet af DNA
- Gør muld til myrebakker:Myrebakker forbedrer jordens fugtighed
- Hvad svarer Celsius til -40 F?


