Hvad sker der med partikler i et stof, når temperaturstigningen?
1. Øget kinetisk energi: Partiklerne bevæger sig hurtigere. De vibrerer mere kraftigt i faste stoffer og væsker, og de bevæger sig mere frit rundt i gasser.
2. Øget potentiel energi: Partiklerne spredte sig længere fra hinanden. Dette gælder især i gasser, hvor partiklerne har mere frihed til at bevæge sig rundt. I faste stoffer kan den øgede energi få partiklerne til at vibrere med større amplitude, hvilket fører til en lille ekspansion.
Her er en oversigt over, hvordan dette påvirker forskellige stoftilstande:
faste stoffer:
* Øget vibration: Partiklerne vibrerer mere kraftigt, hvilket fører til en lille udvidelse af det faste stof.
* smeltning: Hvis temperaturen stiger tilstrækkeligt, får partiklerne nok energi til at overvinde kræfterne, der holder dem i en fast gitterstruktur. Dette resulterer i en faseændring fra fast til væske.
væsker:
* Øget bevægelse: Partiklerne bevæger sig mere frit, hvilket fører til et fald i viskositet (modstand mod flow).
* fordampning: Hvis temperaturen stiger tilstrækkeligt, får partiklerne nok energi til at overvinde kræfterne, der holder dem sammen i flydende tilstand. Dette resulterer i en faseændring fra væske til gas.
Gasser:
* Øget hastighed: Partiklerne bevæger sig hurtigere, hvilket fører til et højere tryk.
* udvidelse: Partiklerne spredte sig længere fra hinanden, hvilket førte til et fald i densitet.
Kortfattet:
* Forøgelse af temperaturen fører til en stigning i kinetisk og potentiel energi af partikler i et stof.
* Dette øgede energi manifesterer sig i hurtigere bevægelse, øget afstand mellem partikler og potentielle faseændringer.
* De specifikke effekter på stoffet afhænger af dets oprindelige tilstand (fast, flydende, gas) og størrelsen af temperaturstigningen.
 Varme artikler
Varme artikler
-
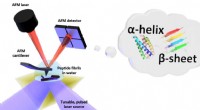 Formen i vand:Første nanoskalamålinger af biomolekylefoldning i væskeSkematisk af opsætningen for fototermisk induceret resonans (PTIR), som inkluderer en infrarød laserkilde og atomic force microscope (AFM) cantilever med en skarp spids, der rører prøven og vibrerer s
Formen i vand:Første nanoskalamålinger af biomolekylefoldning i væskeSkematisk af opsætningen for fototermisk induceret resonans (PTIR), som inkluderer en infrarød laserkilde og atomic force microscope (AFM) cantilever med en skarp spids, der rører prøven og vibrerer s -
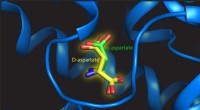 Montering af en højre hånd i en venstrehåndsvanteDenne illustration viser L- og D-aspartat på bindingsstedet for transportproteinet. Kredit:Valentina Arkhipova, University of Groningen Mange biomolekyler findes i to versioner, der er hinandens s
Montering af en højre hånd i en venstrehåndsvanteDenne illustration viser L- og D-aspartat på bindingsstedet for transportproteinet. Kredit:Valentina Arkhipova, University of Groningen Mange biomolekyler findes i to versioner, der er hinandens s -
 Forskere analyserer de kemiske bindinger, der former proteinerIkke-kovalente interaktioner. Kredit:Kamran Makhmudov En international gruppe af forskere, herunder gæsteprofessor fra RUDN Universitet Kamran Makhmudov, har analyseret kemiske bindinger i protein
Forskere analyserer de kemiske bindinger, der former proteinerIkke-kovalente interaktioner. Kredit:Kamran Makhmudov En international gruppe af forskere, herunder gæsteprofessor fra RUDN Universitet Kamran Makhmudov, har analyseret kemiske bindinger i protein -
 Brændselscelle fremme et frisk pust til fremtidigt kraftalternativFast oxid brændselsceller kan bruges i en række forskellige applikationer, herunder effektiv generering af primær- eller nødstrømforsyning til bygninger. En gruppe Bloom Energy-servere genererer strøm
Brændselscelle fremme et frisk pust til fremtidigt kraftalternativFast oxid brændselsceller kan bruges i en række forskellige applikationer, herunder effektiv generering af primær- eller nødstrømforsyning til bygninger. En gruppe Bloom Energy-servere genererer strøm
- Sub gør hurtig opstigning i Det Indiske Ocean; besætningen sikker
- Hvordan dannes ikke -vulkanske bjerge?
- Balletdansere i sensordragter:Ny forskning undersøger, hvordan dans bruges som kommunikationsform
- Hvilken del af jorden modtager mest solenergi?
- Hvorfor var udviklingen af nukleinsyrer vigtig for protoceller?
- Her er et tip:Indrykket cement viser unikke egenskaber


