Hvorfor udtrykkes volumen af gasser i gram DM-3 snarere end CM-3?
Her er hvorfor:
* gram pr. Kubik decimeter (g dm⁻³) repræsenterer densitet , som er massen af et stof pr. Enhedsvolumen. Mens densitet er en vigtig egenskab, er det ikke den primære måde at udtrykke mængden af gasser på.
* mol pr. Kubik decimeter (mol dm⁻³) eller mol pr. Liter (mol l⁻¹) repræsenterer molskoncentration , som er antallet af mol et stof pr. Enhedsvolumen. Molskoncentration er en mere nyttig enhed til at arbejde med gasser, fordi den giver mulighed for direkte sammenligning af mængden af gas, der er til stede i forskellige volumener.
Her er et eksempel:
Lad os sige, at du har 1 mol af en ideel gas ved standardtemperatur og tryk (STP). Denne gas besætter et volumen på 22,4 liter. Den molære koncentration af denne gas ville være 1 mol/22,4 L, hvilket er ca. 0,045 mol L⁻¹.
Sammenfattende bruges g Dm⁻³ til at udtrykke densitet, mens mol dm⁻³ eller mol l⁻¹ bruges til at udtrykke molskoncentration, hvilket er mere relevant for at arbejde med gasser.
Sidste artikelEr kulstof en fast flydende gas eller plasma?
Næste artikelHvilket Archimedes -princip kan anvendes på gasser?
 Varme artikler
Varme artikler
-
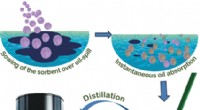 Et organogelator-cellulose-kompositmateriale til praktisk og miljøvenlig genopretning af marine oli…Kredit:Wiley Spildt råolie har gentagne gange forurenet og endda ødelagt marine økosystemer. En effektiv foranstaltning ville være at fjerne spildte oliepletter ved absorption i en adskillelig fas
Et organogelator-cellulose-kompositmateriale til praktisk og miljøvenlig genopretning af marine oli…Kredit:Wiley Spildt råolie har gentagne gange forurenet og endda ødelagt marine økosystemer. En effektiv foranstaltning ville være at fjerne spildte oliepletter ved absorption i en adskillelig fas -
 En vandspaltende katalysator ulig nogen andenKredit:CC0 Public Domain Elektricitet kan genereres af vedvarende kilder som sollys og vind, derefter brugt til at spalte vand, som gør brint som brændstof til nye energienheder såsom brændselscel
En vandspaltende katalysator ulig nogen andenKredit:CC0 Public Domain Elektricitet kan genereres af vedvarende kilder som sollys og vind, derefter brugt til at spalte vand, som gør brint som brændstof til nye energienheder såsom brændselscel -
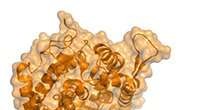 Hvordan tre mutationer arbejder sammen for at anspore til nye SARS-CoV-2-varianterForskerne testede, hvordan tre mutationer ændrede interaktionen mellem en vigtig del af virussen (grå) og det humane protein, som den binder sig til (orange). Kredit:Biochemistry 2022 Som stormbølg
Hvordan tre mutationer arbejder sammen for at anspore til nye SARS-CoV-2-varianterForskerne testede, hvordan tre mutationer ændrede interaktionen mellem en vigtig del af virussen (grå) og det humane protein, som den binder sig til (orange). Kredit:Biochemistry 2022 Som stormbølg -
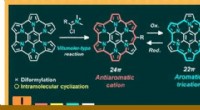 Nitrogen-indlejret polycyklisk forbindelse med stærk antiaromaticitet og stabilitetSyntese af antiaromatisk ekspanderet azacoronen via intramolekylær reaktion af Vilsmeier-typen, som viser aromaticitetsskift ved redoxstimuli. Kredit:American Chemical Society Nitrogen-indlejrede
Nitrogen-indlejret polycyklisk forbindelse med stærk antiaromaticitet og stabilitetSyntese af antiaromatisk ekspanderet azacoronen via intramolekylær reaktion af Vilsmeier-typen, som viser aromaticitetsskift ved redoxstimuli. Kredit:American Chemical Society Nitrogen-indlejrede
- ATLAS -eksperiment undersøger, hvordan Higgs -bosonen interagerer med andre bosoner
- Større forskningssammenslutninger indsender amicus-kort fra Højesteret til støtte for racebevidst…
- Hvad er termonisk emission?
- Ved hvilken hastighed rejser magnetisk stråling?
- Hvilken gas findes i plante- og dyrevæv?
- Er Red Giant en stjerne eller type stjerne?


