Hvorfor kan du squash gasser, men ikke faste stoffer?
Gasser:
* meget komprimerbar: Gasser har meget store mellemrum mellem deres molekyler. Når du anvender tryk, reduceres disse rum, hvilket får volumenet af gassen til at falde markant. Tænk på at klemme en ballon - du komprimerer luften inde.
* Ingen fast form eller volumen: Gasmolekyler bevæger sig frit og tager formen på deres beholder. Dette gør det muligt for dem at komprimeres let.
faste stoffer:
* relativt ukomprimerbar: Faststoffer har deres molekyler pakket meget tæt sammen, med stærke bindinger, der holder dem på plads. Påføring af tryk på et solidt reducerer kun lidt mellemrum mellem molekyler. Dette resulterer i en meget mindre ændring i volumen sammenlignet med gasser.
* Fast form og volumen: Faststoffer opretholder deres form og volumen uanset den beholder, de er i. Dette gør dem mindre komprimerbare.
Kortfattet:
* Gasser er komprimerbare, fordi deres molekyler er vidt adskilt og bevæger sig frit, hvilket gør det muligt for dem at blive presset sammen.
* faste stoffer er mindre komprimerbare, fordi deres molekyler er tæt pakket og stærkt bundet, hvilket gør det vanskeligt at skubbe dem tættere sammen.
Vigtig note: Mens vi generelt tænker på faste stoffer som ukomprimerbart, kan meget høje tryk deformere og endda ændre strukturen af nogle faste stoffer.
Sidste artikelHvad er de subatomære partikler af jern?
Næste artikelHvilket metal er den næstbedste dirigent?
 Varme artikler
Varme artikler
-
 Forskere rekrutterer nye atomare sværvægtere i målrettet kamp mod kræftKatherine Shield (fra venstre), Dahlia An, Tyler Bailey på Lawrence Berkeley National Laboratory tirsdag, 17. november kl. 2020, i Berkeley, Californien Kredit:Marilyn Sargent/Berkeley Lab En love
Forskere rekrutterer nye atomare sværvægtere i målrettet kamp mod kræftKatherine Shield (fra venstre), Dahlia An, Tyler Bailey på Lawrence Berkeley National Laboratory tirsdag, 17. november kl. 2020, i Berkeley, Californien Kredit:Marilyn Sargent/Berkeley Lab En love -
 Brug af skovens naturlige evne til at bøje sig ved tørring for at skabe buede strukturerUrbach-tårnet, en 14 m høj bygningsdemonstrator med høj krumning CLT-komponenter fremstillet ved hjælp af selvformende fremstillingsteknologi. Kredit:ICD/ITKE Universitetet i Stuttgart Et team af
Brug af skovens naturlige evne til at bøje sig ved tørring for at skabe buede strukturerUrbach-tårnet, en 14 m høj bygningsdemonstrator med høj krumning CLT-komponenter fremstillet ved hjælp af selvformende fremstillingsteknologi. Kredit:ICD/ITKE Universitetet i Stuttgart Et team af -
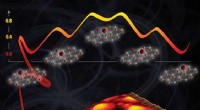 At placere atomer til optimale katalysatorerPå toppen af en grafenplade kastet som et tæppe over en rutheniummetaloverflade, oxygenatomer (røde kugler på øverste billede, små ujævnheder på nederste billede) ændre deres bindingspræference til
At placere atomer til optimale katalysatorerPå toppen af en grafenplade kastet som et tæppe over en rutheniummetaloverflade, oxygenatomer (røde kugler på øverste billede, små ujævnheder på nederste billede) ændre deres bindingspræference til -
 At gøre polyurethan nedbrydeligt giver dets komponenter et nyt livDet nedbrydelige polyurethanmateriale (lyserød strimmel) kvælder og opløses derefter i syre blandet med et organisk opløsningsmiddel (venstre hætteglas på begge billeder), men ikke når det placeres i
At gøre polyurethan nedbrydeligt giver dets komponenter et nyt livDet nedbrydelige polyurethanmateriale (lyserød strimmel) kvælder og opløses derefter i syre blandet med et organisk opløsningsmiddel (venstre hætteglas på begge billeder), men ikke når det placeres i
- Hvad er forskellen i tyngdekraften et objekt med en masse 23,5 kg og 14,7 kg?
- Hvordan formede gamle bakterier vores planet?
- Et medlem af Sporozoan Group Protists er?
- Kan du give mig mindst 10 apparater, der bruger termisk energi med billede?
- Hvad er svaret på forbliver eller et indtryk af et planetdyr, der eksisterede i tidligere geologisk…
- Metode til fremstilling af svovlforbindelser i celler viser løfte om vævsreparation


