Hvad er elektronkonfigurationen af Iron II?
1. Neutral jern (Fe):
* Jern har et atomnummer på 26, hvilket betyder, at det har 26 protoner og 26 elektroner.
* Dens elektronkonfiguration er: 1S² 2S² 2P⁶ 3S² 3P⁶ 4S² 3D⁶
2. Jern (ii) ion (fe²⁺):
* Jern (II) formularer ved at miste to elektroner.
* Disse elektroner går tabt fra det højeste energiniveau, som er 4S Orbital.
* Elektronkonfigurationen af Fe²⁺ bliver: 1S² 2S² 2P⁶ 3S² 3P⁶ 3d⁶
Derfor er elektronkonfigurationen af jern (II):1S² 2S² 2P⁶ 3S² 3P⁶ 3d⁶
Sidste artikelHvad ville være produktet af beta -forfald Bismuth?
Næste artikelHvilke ændringer ledsager en nuklear reaktion?
 Varme artikler
Varme artikler
-
 Oprettelse af mRNA med en helt kemisk proces kan give mulighed for tilpassede mRNA-vaccinermRNA med sin glødende hætte. Kredit:Reiko Matsushita Forskere ved Nagoya University i Japan har udviklet en ny kemisk proces, der kan repræsentere et vigtigt gennembrud i at skabe skræddersyede mRN
Oprettelse af mRNA med en helt kemisk proces kan give mulighed for tilpassede mRNA-vaccinermRNA med sin glødende hætte. Kredit:Reiko Matsushita Forskere ved Nagoya University i Japan har udviklet en ny kemisk proces, der kan repræsentere et vigtigt gennembrud i at skabe skræddersyede mRN -
 En solenergi-drevet bæredygtig proces til syntese af ethylenglycol fra methanolDirekte fotokatalytisk kobling af methanol til ethylenglycol (EG) er yderst attraktiv. Den første metaloxidfotokatalysator, tantalbaseret halvleder, er rapporteret for foretrukken aktivering af C-H-bi
En solenergi-drevet bæredygtig proces til syntese af ethylenglycol fra methanolDirekte fotokatalytisk kobling af methanol til ethylenglycol (EG) er yderst attraktiv. Den første metaloxidfotokatalysator, tantalbaseret halvleder, er rapporteret for foretrukken aktivering af C-H-bi -
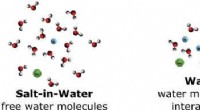 Højkoncentrerede vandige elektrolytter kunne erstatte opløsningsmidler, der bruges i batterierGrafisk abstrakt. Kredit: Aktuel mening i elektrokemi https://doi.org/10.1016/j.coelec.2020.01.006 Højkoncentrerede vandige elektrolytter, kendt som vand-i-salt elektrolytter, kunne være et alter
Højkoncentrerede vandige elektrolytter kunne erstatte opløsningsmidler, der bruges i batterierGrafisk abstrakt. Kredit: Aktuel mening i elektrokemi https://doi.org/10.1016/j.coelec.2020.01.006 Højkoncentrerede vandige elektrolytter, kendt som vand-i-salt elektrolytter, kunne være et alter -
 Forskning giver håb om enklere kræftdiagnose og behandlingRyan Kelly i sit laboratorium. Kredit:Jaren Wilkey/BYU Overvågning af kræft kan ofte være en påtrængende og udmattende proces for patienter. Men med Brigham Young University kemiprofessor Ryan Kel
Forskning giver håb om enklere kræftdiagnose og behandlingRyan Kelly i sit laboratorium. Kredit:Jaren Wilkey/BYU Overvågning af kræft kan ofte være en påtrængende og udmattende proces for patienter. Men med Brigham Young University kemiprofessor Ryan Kel
- Hvilken funktion har målt bølgelængde på 550 nm?
- Hvilke materialer transmitterer let let?
- Hvorfor har de 4 resulterende celler af meiose ikke parret kromosomer?
- Hvorfor ser det ud til, at solen stiger i øst og sætter vest?
- Hvad er mønstre på tværs af periode 3 pH af vandige chloridopløsninger?
- Vil en rød gigantisk stjerne ende som supernova?


