Hvilke egenskaber ved metaller og saltvand gør dem til gode materialer til et batteri?
Metaller:
* Konduktivitet: Metaller er fremragende ledere af elektricitet. Dette giver mulighed for den lette strøm af elektroner gennem batterikredsløbet.
* Elektrokemisk reaktivitet: Forskellige metaller har forskellige tendenser til at miste eller få elektroner (deres elektrokemiske potentiale). Denne forskel i reaktivitet er vigtig for at drive strømmen af elektroner og skabe elektrisk energi.
* stabilitet: Mange metaller er stabile og modstandsdygtige over for korrosion og sikrer batteriets langsigtede ydelse.
saltvand (elektrolyt):
* ionisk ledningsevne: Saltvandsløsninger indeholder ioner (ladede partikler), der kan bevæge sig frit. Disse ioner fungerer som ladningsbærere, hvilket tillader strøm af elektricitet inden for elektrolytten.
* Kemisk reaktivitet: Elektrolytten interagerer med metalelektroderne, letter overførslen af elektroner og afsluttede kredsløbet.
* opløsningsmiddelegenskaber: Saltvand opløser salte og andre kemikalier, hvilket skaber et miljø, der er befordrende for elektrokemiske reaktioner.
Hvordan disse egenskaber fungerer sammen i et batteri:
1. Elektroder: Batteriet bruger to forskellige metaller (f.eks. Zink og kobber) som elektroder. Disse metaller har forskellige elektrokemiske potentialer, hvilket betyder, at man let mister elektroner (anode), mens den anden let får elektroner (katode).
2. elektrolyt: Elektrolytten er en saltvandopløsning, der giver ionerne mulighed for at bevæge sig frit.
3. Elektronstrøm: Når kredsløbet er lukket, strømmer elektroner fra anoden (mere reaktivt metal) til katoden (mindre reaktivt metal) gennem det ydre kredsløb.
4. Kemiske reaktioner: Samtidig forekommer kemiske reaktioner inden for elektrolytten, hvor ioner vandrer til elektroderne for at afbalancere elektronoverførslen.
Nøglepunkter:
* Metalvalg er afgørende: Forskellige metalkombinationer skaber forskellige batterispændinger og effektkapaciteter.
* Elektrolytkoncentration og salttype: Disse faktorer påvirker batteriets ydelse og levetid.
* Elektrolytten skal være ledende, men ikke reaktiv nok til at forårsage hurtig korrosion af elektroderne.
I det væsentlige muliggør kombinationen af metaller med deres ledningsevne og elektrokemisk reaktivitet sammen med den ioniske ledningsevne og kemiske egenskaber ved saltvand i stand til omdannelse af kemisk energi til elektrisk energi i et batteri.
Sidste artikelHvad er aktiviteten af et radioaktivt stof?
Næste artikelGiv et navn på stof, der kunne bruges til at neutralisere vandet?
 Varme artikler
Varme artikler
-
 Samarbejde giver lovende innovation inden for pletbestandighedPrøver af klud både ubehandlet, venstre, og behandlet med en fluor-fri oleofob belægning udviklet i laboratorier af Emmanuel Giannelis, professor i materialevidenskab og teknik, og Jintu Fan, professo
Samarbejde giver lovende innovation inden for pletbestandighedPrøver af klud både ubehandlet, venstre, og behandlet med en fluor-fri oleofob belægning udviklet i laboratorier af Emmanuel Giannelis, professor i materialevidenskab og teknik, og Jintu Fan, professo -
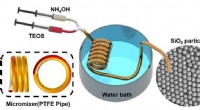 Forskere bruger et teflonrør til at lave en billig, simpel reaktor til silicapartikelsynteseEksperimentel opsætning af mikrofluidisk mixer til syntese af silica. Kredit:Yang Hui Forskere i Australien og Kina har foreslået en innovativ og omkostningseffektiv ny metode til at skabe silicap
Forskere bruger et teflonrør til at lave en billig, simpel reaktor til silicapartikelsynteseEksperimentel opsætning af mikrofluidisk mixer til syntese af silica. Kredit:Yang Hui Forskere i Australien og Kina har foreslået en innovativ og omkostningseffektiv ny metode til at skabe silicap -
 Næste generations insektmidler til at bekæmpe myggebårne sygdommeAnopheles gambiae myg, lever af blod. Kredit:James Gathany, Centre for Disease Control and Prevention Næsten 700 millioner mennesker lider af myggebårne sygdomme – såsom malaria, West Nile, Zika-
Næste generations insektmidler til at bekæmpe myggebårne sygdommeAnopheles gambiae myg, lever af blod. Kredit:James Gathany, Centre for Disease Control and Prevention Næsten 700 millioner mennesker lider af myggebårne sygdomme – såsom malaria, West Nile, Zika- -
 Oksekødspeptider blokerer for bitter smagKredit:American Chemical Society Fra burgere til bøffer, oksekød har en lang historie for at være en lækker del af aftensmaden. Men hvad nu hvis den behagelige oplevelse med at spise oksekød kunne
Oksekødspeptider blokerer for bitter smagKredit:American Chemical Society Fra burgere til bøffer, oksekød har en lang historie for at være en lækker del af aftensmaden. Men hvad nu hvis den behagelige oplevelse med at spise oksekød kunne
- Undersøgelse demonstrerer spektrografinstrumentets evne til at kortlægge månesammensætningen
- Hvor danner de fleste bjergbælter?
- Tilpasninger i Moths
- Dental emalje undersøgelse tyder på forskelle i neandertaler og palæolitisk menneskelig barndom s…
- Hvad betyder det, hvis luften er mættet?
- Er videnskabelig metode teoretiseret, at planeter flyttes i ovale stier rundt om solen?


