Er tætheden af væske den samme som gas?
* Intermolekylære kræfter: Væsker har stærkere intermolekylære kræfter (kræfter mellem molekyler) end gasser. Disse kræfter holder molekylerne tættere sammen i en væske, hvilket resulterer i et tættere arrangement.
* Kompressibilitet: Gasser er meget komprimerbare, hvilket betyder, at deres molekyler kan presses tættere sammen. Væsker er meget mindre komprimerbare.
* afstand: Molekylerne i en gas er langt fra hinanden, mens molekylerne i en væske er meget tættere sammen.
Tænk på det på denne måde: Forestil dig et værelse fyldt med mennesker. Hvis alle står langt fra hinanden, har rummet en lav densitet. Hvis alle er pakket tæt sammen, har rummet en høj densitet. Væsker er som det pakket rum, mens gasser er som rummet med mennesker spredt ud.
Sidste artikelHvilken væske har den letteste densitet?
Næste artikelHvorfor genereres hverken ilt eller NADPH ved cyklisk elektronstrøm?
 Varme artikler
Varme artikler
-
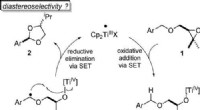 Forskere udvikler en bæredygtig katalyseprocesAtomøkonomisk omdannelse af benzylethere til acetaler ved titanocen(III)-katalyse i enkeltelektrontrin (SET). Angewandte Chemie, DOI:10.1002/anie.202013561 Acetaler er vigtige kemiske forbindelser
Forskere udvikler en bæredygtig katalyseprocesAtomøkonomisk omdannelse af benzylethere til acetaler ved titanocen(III)-katalyse i enkeltelektrontrin (SET). Angewandte Chemie, DOI:10.1002/anie.202013561 Acetaler er vigtige kemiske forbindelser -
 Superdiamond carbon-bor bure kan fange og udnytte forskellige egenskaberKlatratstrukturen af todelt sodalit-type, som består af trunkerede oktaedriske værts-bure, der fanger strontium-gæste-atomer, blev syntetiseret under højtryks- og højtemperaturforhold ved hjælp af e
Superdiamond carbon-bor bure kan fange og udnytte forskellige egenskaberKlatratstrukturen af todelt sodalit-type, som består af trunkerede oktaedriske værts-bure, der fanger strontium-gæste-atomer, blev syntetiseret under højtryks- og højtemperaturforhold ved hjælp af e -
 Forståelse af relaxor ferroelektriske egenskaber kan føre til mange fremskridtChirale (spejl) molekyler giver relaxor ferroelektriske stoffer deres fantastiske egenskaber. Kredit:MR, Penn State En ny grundlæggende forståelse af polymer relaxor ferroelektrisk adfærd kan føre
Forståelse af relaxor ferroelektriske egenskaber kan føre til mange fremskridtChirale (spejl) molekyler giver relaxor ferroelektriske stoffer deres fantastiske egenskaber. Kredit:MR, Penn State En ny grundlæggende forståelse af polymer relaxor ferroelektrisk adfærd kan føre -
 At møde en 100 år gammel udfordring kan føre vejen til digitale aromaerLugte kan måles ved deres afstand fra hinanden. Kredit:Weizmann Institute of Science Dufte – der lover mystik og intriger – blandes af mesterparfumører, deres opskrifter holdt hemmelige. I en ny u
At møde en 100 år gammel udfordring kan føre vejen til digitale aromaerLugte kan måles ved deres afstand fra hinanden. Kredit:Weizmann Institute of Science Dufte – der lover mystik og intriger – blandes af mesterparfumører, deres opskrifter holdt hemmelige. I en ny u
- Hvorfor klassificeres hastighed som en skalær mængde og hastighed klassificeret vektormængde?
- Udtryk dig selv:Forskere bruger genetisk algoritme til at designe selvsamlende ssDNA-podede partikle…
- Hvad ulves tænder afslører om deres liv
- Forskning inspicerer emissionen fra millisekund pulsar PSR J0218+4232
- Hvad er et konstant volumengastermometer?
- Forskere afslører, at boliger i flodsletter er overvurderet med næsten 44 milliarder dollars


