Forskere udvikler en bæredygtig katalyseproces
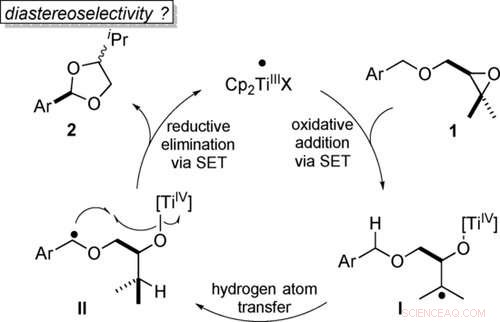
Atomøkonomisk omdannelse af benzylethere til acetaler ved titanocen(III)-katalyse i enkeltelektrontrin (SET). Angewandte Chemie, DOI:10.1002/anie.202013561
Acetaler er vigtige kemiske forbindelser, der bruges, for eksempel, i produktionen af visse medicinske midler. En ny metode gør nu deres syntese lettere og mere miljøvenlig. Kemikere ved universitetet i Bonn har udviklet og optimeret den bæredygtige katalytiske proces. Der blev også brugt state-of-the-art computersimuleringer. Reaktionen er baseret på en mekanisme, der ofte forekommer i naturen, men har sjældent været brugt i kemisk syntese indtil nu. Resultaterne offentliggøres i tidsskriftet Angewandte Chemie .
Nøgletrinet i produktionen af acetaler er bindingen af to oxygenatomer til et kulstofatom. Kemikere opnår ofte dette arrangement med oxidation. Normalt bruges stærke oxidationsmidler til at opnå dette ved at frigive et oxygenatom under reaktionen. Resten af oxidationsmidlet skal bortskaffes efter syntesen.
"I vores undersøgelse, imidlertid, vi beskriver en vej, der omtales som atom-økonomisk, hvilket betyder, at det ikke genererer affald, " forklarer prof. Dr. Andreas Gansäuer fra Kekulé Institut for Organisk Kemi og Biokemi ved Universitetet i Bonn. "Udgangsmolekylet i sig selv indeholder allerede det oxygenatom, der kræves til oxidation. Den katalyse, vi har udviklet, flytter simpelthen denne ilt i molekylet, som skaber acetalen."
Udgangsmolekylet indeholder en såkaldt epoxygruppe, en slags "trekant", hvor to hjørner er dannet af kulstofatomer og det tredje af et oxygenatom. Sådanne tredobbelte ringe er under stor spænding og går derfor let fra hinanden ved oxygenatomet. Epoxy lagrer den nødvendige reaktionsenergi som en komprimeret fjeder.
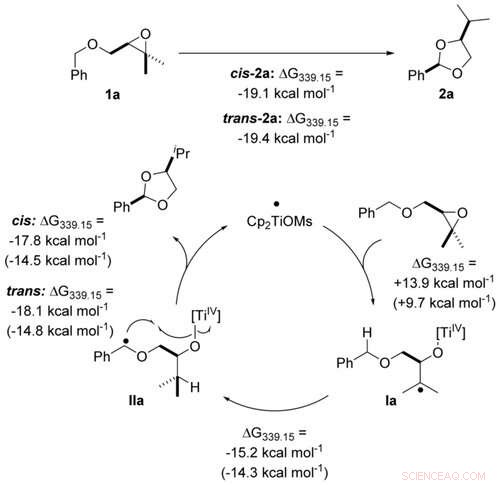
Atomøkonomisk transformation af benzylethere til acetaler ved titanocen(III)-katalyse i enkeltelektrontrin beregnet ved PW6B95-D4/def2-QZVP + COSMO-RS(THF)// PBEh-3c/DCOSMO-RS(THF) niveau. Værdier inden for parentes beregnes for katalysatoren Cp2TiCl. Angewandte Chemie, DOI:10.1002/anie.202013561
Katalyse baseret på naturens model
For at nå dette mål kræves en passende katalysator. I overført betydning, iltatomer har to "arme", som de kan danne bindinger med. Hvis epoxyringen går i stykker, en af disse arme bliver fri. Katalysatoren binder nu midlertidigt til den. Dette initierer en sekvens af molekyle-interne (intramolekylære) omlejringer. I slutningen af denne sekvens, oxygenatomet frigiver katalysatoren igen og binder sig i stedet til det ønskede kulstof. "Dette trin kaldes oxygen rebound, " siger Gansäuer.
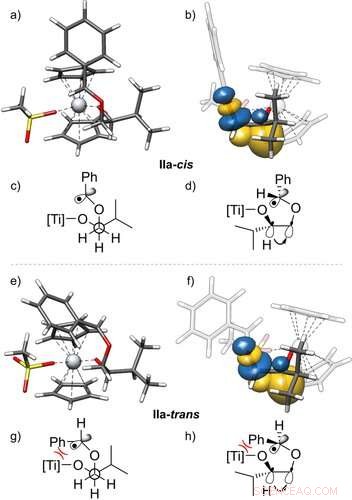
3D-strukturer af radikalerne IIa-cis (a, b) og IIa -trans (e, f) og deres stabilisering ved gauche-interaktioner, med sideudsigt. De viste naturlige bindingsorbitaler (NBO)23 er opnået fra en PBEh‐3c+CPCM(THF) beregning. Derudover Newman projektioner (c, g) og kile- og stregstrukturer (d, h) af disse radikaler er givet. De viser C -H -bindingsorbitalen, der donerer til σ*-orbitalen af C -O -bindingen, visualisering af gauche-effekten. Kun én af to effektive gauche-interaktioner er vist. Isosoverfladeværdi =0,05 e − 1/2 bohr − 3/2. Angewandte Chemie, DOI:10.1002/anie.202013561
Denne mekanisme har hidtil sjældent været brugt i kemiske synteser - ganske ulig i naturen:Leveren, for eksempel, bruger "iltrebound" til at nedbryde toksiner. Dette kræver også katalysatorer, de såkaldte P450-enzymer. Deres aktive center indeholder et jernatom. "Hjertet i vores katalysator består også af et almindeligt og ikke-giftigt metal, nemlig titanium, " forklarer prof. dr. Stefan Grimme fra Institut for Fysisk og Teoretisk Kemi ved Universitetet i Bonn.
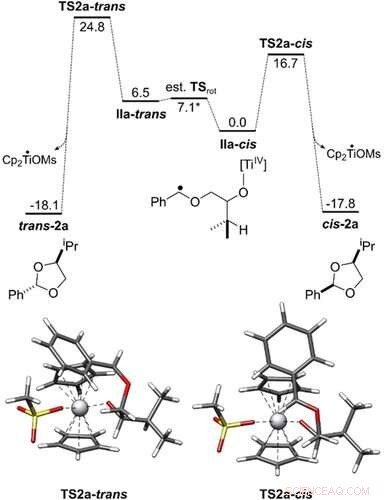
Energiprofil for omdannelsen af IIa‐cis og IIa‐trans til cis‐2 a og trans‐2 a. Alle Gibbs frie energier er vist i kcal mol−1. Overgangsstatens geometrier blev opnået med PBEh ‐ 3c/COSMO (THF). Den katalytiske cyklus er blevet undersøgt på PW6B95-D4/def2-QZVP + COSMO-RS(THF)// PBEh-3c/ COSMO(THF) teoriniveau. Angewandte Chemie, DOI:10.1002/anie.202013561
Katalysator tuning på computeren
Under acetalsyntese, titan absorberer først et oxygenatom og frigiver det derefter igen (oxidation efterfølges af en såkaldt reduktion). Dette virker kun effektivt, hvis det binder ilten stærkt nok til sig selv uden at "klæbe" sig for meget. For at justere dets iltaffinitet passende, titanium er bundet til visse molekyler, dens ligander. Afhængig af den forpligtende partner, metallet har da en noget stærkere oxiderende virkning eller kan nemmere reduceres. De bedst egnede "tuning-molekyler" udvælges i dag ved hjælp af en computer. Forskergruppen omkring prof. Grimme har specialiseret sig i denne opgave:I de senere år det har udviklet algoritmer, der tillader meget hurtige simuleringer af katalysatoregenskaber.
Dette gjorde det muligt for forskerne i deres undersøgelse at optimere deres katalysator, så den fuldstændigt omdanner udgangsmaterialet til den ønskede acetal. "Resultatet dokumenterer meget pænt, hvor nyttigt tæt samarbejde mellem eksperiment og teori er til udvikling af bæredygtige katalysemetoder, " siger Gansäuer.
 Varme artikler
Varme artikler
-
 Materialer til brintservice avanceret af nyt multilab-konsortiumBrendan Davis, hoveddesigner og operatør af højtryksmekaniske testsystemer i Hydrogen Effects on Materials Laboratory ved Sandia National Laboratories, udarbejder et system til test med brintgas. Kred
Materialer til brintservice avanceret af nyt multilab-konsortiumBrendan Davis, hoveddesigner og operatør af højtryksmekaniske testsystemer i Hydrogen Effects on Materials Laboratory ved Sandia National Laboratories, udarbejder et system til test med brintgas. Kred -
 Hvordan en interesse for bipolar lidelse førte til en bedre forståelse af leukæmiEt nyt projekt afslører, at enzymet GSK-3, et mål for stemningslidelsen stoffet lithium, har en rolle i at kontrollere alternativ splejsning i celler. Denne observation kan give indsigt i leukæmi. Kre
Hvordan en interesse for bipolar lidelse førte til en bedre forståelse af leukæmiEt nyt projekt afslører, at enzymet GSK-3, et mål for stemningslidelsen stoffet lithium, har en rolle i at kontrollere alternativ splejsning i celler. Denne observation kan give indsigt i leukæmi. Kre -
 Forskere finder lovende nanopartikelkandidater til kuldioxidopsamling og omdannelseOriginalt kunstværk fra University of Pittsburgh, der viser en kobberbaseret bimetallisk nanopartikel designet til at adsorbere og aktivere kuldioxid, dukkede op på forsiden af ChemSusChem i april 2
Forskere finder lovende nanopartikelkandidater til kuldioxidopsamling og omdannelseOriginalt kunstværk fra University of Pittsburgh, der viser en kobberbaseret bimetallisk nanopartikel designet til at adsorbere og aktivere kuldioxid, dukkede op på forsiden af ChemSusChem i april 2 -
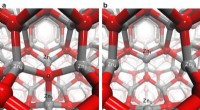 Det er en fælde - Forskere identificerer processen, hvorved huller bliver fanget i ZnO nanopartikle…Argonne-forskere hjalp med at identificere den proces, hvorved huller bliver fanget i nanopartikler lavet af zinkoxid, et materiale af potentiel interesse til solenergianvendelser, fordi det absorbere
Det er en fælde - Forskere identificerer processen, hvorved huller bliver fanget i ZnO nanopartikle…Argonne-forskere hjalp med at identificere den proces, hvorved huller bliver fanget i nanopartikler lavet af zinkoxid, et materiale af potentiel interesse til solenergianvendelser, fordi det absorbere
- Menneskelig adfærd:hvad videnskabsmænd har lært om det fra pandemien
- Principper for en grøn kemifremtid
- Forskning tyder på, at der er en bedre måde at undervise universitetsstuderende i fysik på
- Simple indgreb kan hjælpe folk med at få øje på falske overskrifter
- Miljø:Skift fra små til mellemstore plastikflasker kan reducere PET-affald
- Specifikationer for E-Z-Go Engine


