Hvad er elektronkonfigurationen af aluminium?
1S² 2S² 2P⁶ 3S² 3P¹
Her er en sammenbrud:
* 1S²: Det første energiniveau (n =1) har 2 elektroner i S -orbitalen.
* 2s²: Det andet energiniveau (n =2) har 2 elektroner i S -orbitalen.
* 2p⁶: Det andet energiniveau har også 6 elektroner i P orbital.
* 3S²: Det tredje energiniveau (n =3) har 2 elektroner i S -orbitalen.
* 3p¹: Det tredje energiniveau har 1 elektron i P orbital.
Vigtig note: Aluminium har 13 elektroner, som indikeret af dets atomnummer. Denne elektronkonfiguration følger AUFBAU -princippet og påfylder orbitaler i rækkefølge af stigende energi.
Sidste artikelHvad er tætheden af ædelgasser?
Næste artikelHvordan kan varmeoverførsel i væsker og gasser reduceres?
 Varme artikler
Varme artikler
-
 Undersøgelse bekræfter høj strålingsmodstand af højentropi-karbidkeramikKredit:Journal of the European Ceramic Society (2022). DOI:10.1016/j.jeurceramsoc.2022.01.061 En ny undersøgelse om bestrålingsevaluering af højentropi carbid keramik (HECCer) har påvist deres bemæ
Undersøgelse bekræfter høj strålingsmodstand af højentropi-karbidkeramikKredit:Journal of the European Ceramic Society (2022). DOI:10.1016/j.jeurceramsoc.2022.01.061 En ny undersøgelse om bestrålingsevaluering af højentropi carbid keramik (HECCer) har påvist deres bemæ -
 Turende strukturer i et menneskeskabt interfaceReaktionsdiffusionsprocessen drev dannelsen af den komplicerede uorganiske Turing -struktur. Kredit:ZHANG Xiaolong I 1952, Alan Turing, far til datalogi og kunstig intelligens, foreslået, at vis
Turende strukturer i et menneskeskabt interfaceReaktionsdiffusionsprocessen drev dannelsen af den komplicerede uorganiske Turing -struktur. Kredit:ZHANG Xiaolong I 1952, Alan Turing, far til datalogi og kunstig intelligens, foreslået, at vis -
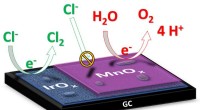 Et skridt nærmere bæredygtig energi fra havvandUnder elektrolyse af vand, elektricitet ledes gennem vandet for at spalte det i andre stoffer. I den ønskede reaktion, flydende vand (H2O) spaltes i oxygengas (O2) og brintgas (H2). I saltvand, natriu
Et skridt nærmere bæredygtig energi fra havvandUnder elektrolyse af vand, elektricitet ledes gennem vandet for at spalte det i andre stoffer. I den ønskede reaktion, flydende vand (H2O) spaltes i oxygengas (O2) og brintgas (H2). I saltvand, natriu -
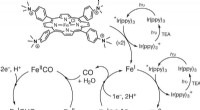 Omdannelse af kuldioxid til metan ved hjælp af jern og sollysSkitse af den foreslåede mekanisme til CO2 -reduktion til CH4 ved katalysator 1. Kredit: Natur (2017). DOI:10.1038/nature23016 (Phys.org) - Et kombineret team af forskere fra Université Paris Did
Omdannelse af kuldioxid til metan ved hjælp af jern og sollysSkitse af den foreslåede mekanisme til CO2 -reduktion til CH4 ved katalysator 1. Kredit: Natur (2017). DOI:10.1038/nature23016 (Phys.org) - Et kombineret team af forskere fra Université Paris Did
- Hvad er ingredienser i frugtsalt?
- Hvilke kræfter har kun indflydelse på objekter, som de berører?
- Hvad vil der ske, hvis energi ødelægges?
- Hvilken faktor påvirker lysstyrken af stjerner?
- Ny enhed i Z-maskine måler kraft til kernefusion
- Sådan narre du en mus:'Kemisk camouflage' kan skjule afgrøder og reducere tab med over 60 %


