Hvad er konjugerede PI -elektroner?
Konjugerede PI -elektroner:En symfoni af binding
Forestil dig en kæde med skiftende enkelt- og dobbeltobligationer. Denne ordning skaber en speciel slags elektronsystem, hvor pi -elektronerne , de involverede i dobbeltbindingen, er delokaliserede over hele kæden. Dette system kaldes konjugerede PI -elektroner .
her er hvad der gør dem specielle:
* delokalisering: I stedet for at være begrænset til en bestemt dobbeltbinding, er PI -elektronerne frit til at bevæge sig over hele det konjugerede system. Dette skaber en sky af elektroner, der strækker sig over alle de involverede atomer.
* stabilitet: Denne delokalisering øger molekylets samlede stabilitet. Elektronerne er mindre tilbøjelige til at blive trukket væk, hvilket gør molekylet mindre reaktivt.
* Unikke egenskaber: Konjugerede systemer udviser unikke egenskaber som:
* Absorption af specifikke bølgelængder af lys: Dette er grunden til, at mange organiske forbindelser med konjugerede systemer er farverige.
* Øget polariserbarhed: De reagerer lettere på tilstedeværelsen af elektriske felter, hvilket gør dem nyttige i elektroniske anvendelser.
* Forbedret elektrisk ledningsevne: Dette er grundlaget for organiske halvledere og andre elektroniske materialer.
Eksempler:
* benzen: Det klassiske eksempel på et konjugeret system. Dens seks PI -elektroner er delokaliseret over hele ringen, hvilket giver den enestående stabilitet.
* polyacetylen: En lang kæde med skiftende enkelt- og dobbeltobligationer. Det konjugerede system giver det mulighed for at udføre elektricitet.
* beta-caroten: Det pigment, der er ansvarligt for den orange farve på gulerødder. Det udvidede konjugerede system absorberer blåt lys, hvilket afspejler orange lys.
Sammenfattende er konjugerede PI -elektroner en nøglefunktion i organisk kemi, der giver molekyler unikke egenskaber og anvendelser. Deres delokalisering og stabilitet er vigtige for at forstå opførsel og funktion af mange vigtige forbindelser.
 Varme artikler
Varme artikler
-
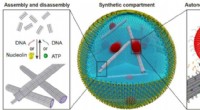 Endnu et skridt mod syntetiske cellerDNA-baserede efterligninger af cytoskeletfilamenter til reversibel samling og lasttransport. Kredit:University of Stuttgart og Max-Planck-Institut for Medical Research At bygge funktionelle synteti
Endnu et skridt mod syntetiske cellerDNA-baserede efterligninger af cytoskeletfilamenter til reversibel samling og lasttransport. Kredit:University of Stuttgart og Max-Planck-Institut for Medical Research At bygge funktionelle synteti -
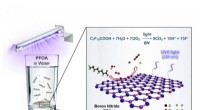 Bornitrid ødelægger for evigt kemikalier PFOA, GenXEn illustration af bornitrid-fotokatalyse, der ødelægger det forurenende stof PFOA i vand. Kredit:Billede udlånt af M. Wong/Rice University Rice University kemiingeniører fandt en effektiv katalys
Bornitrid ødelægger for evigt kemikalier PFOA, GenXEn illustration af bornitrid-fotokatalyse, der ødelægger det forurenende stof PFOA i vand. Kredit:Billede udlånt af M. Wong/Rice University Rice University kemiingeniører fandt en effektiv katalys -
 Elektriske vandpiber er måske ikke sikrere end traditionelle kul-baseredeKredit:American Chemical Society Vandpibetobaksrygning, ellers kendt som vandpibe eller shisha, bliver stadig mere populær over hele verden, især blandt unge. Traditionelle vandpiber brænder træk
Elektriske vandpiber er måske ikke sikrere end traditionelle kul-baseredeKredit:American Chemical Society Vandpibetobaksrygning, ellers kendt som vandpibe eller shisha, bliver stadig mere populær over hele verden, især blandt unge. Traditionelle vandpiber brænder træk -
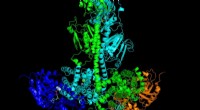 Forskere løser proteinstruktur forbundet med arvelige nethindesygdommeModel af UNH -forskere af det aktiverede kompleks af PDE6 -dimeren (grøn og cyan) med to transducin -underenheder (blå og orange) forbundet med fotoreceptormembranen. Kredit:UNH Forskere ved Unive
Forskere løser proteinstruktur forbundet med arvelige nethindesygdommeModel af UNH -forskere af det aktiverede kompleks af PDE6 -dimeren (grøn og cyan) med to transducin -underenheder (blå og orange) forbundet med fotoreceptormembranen. Kredit:UNH Forskere ved Unive
- Udtrykker gener sig gennem poesi?
- Hvorfor kulstoffri boliger skal lede det grønne opsving fra COVID-19
- Hvorfor kræver mekaniske bølger et medium?
- Hvad sker der for radius, når et atom mister elektron?
- Hvad er samspillet mellem elektriske ladninger og magneter?
- Eksperter:I kølvandet på COVID-19, arbejdsgivere skal gøre kontorer til helbredende rum


