Hvad sker der med den molekylære bevægelse af en væske, når den fryser?
* i en væske: Molekyler er i konstant bevægelse og bevæger sig forbi hinanden frit. De har mere kinetisk energi, hvilket fører til en større gennemsnitlig afstand mellem dem.
* Under frysning: Når temperaturen falder, mister molekylerne kinetisk energi og bremser. Dette får de attraktive kræfter mellem molekyler til at blive mere dominerende. Molekylerne begynder at arrangere sig i en mere ordnet, krystallinsk struktur.
* i en solid (frosset tilstand): Molekylerne er nu tæt pakket i et fast, gentagne arrangement. De vibrerer på plads, men deres bevægelse er meget mere begrænset. Molekylerne har mindre kinetisk energi, end de gjorde i flydende tilstand.
I det væsentlige går molekylerne fra en tilstand af tilfældig bevægelse til en tilstand af bestilt vibration . Denne reducerede molekylære bevægelse er grunden til, at faste stoffer har en fast form og volumen, i modsætning til væsker.
Sidste artikelHvilken generel elektronarrangement er ledende for kemisk inaktivitet?
Næste artikelHvilke materialer er tegn lavet af?
 Varme artikler
Varme artikler
-
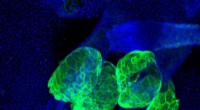 Forskere opdager en ny receptor, der regulerer talgkirtlens stamcellers funktionEmbigin-molekyle (grøn) er stærkt udtrykt i hudcellerne, der differentierer til talgkirtler. Cellernes kerner farves blå; de lange strukturer er hårsække. Kredit:Universitetet i Turku Stamceller og
Forskere opdager en ny receptor, der regulerer talgkirtlens stamcellers funktionEmbigin-molekyle (grøn) er stærkt udtrykt i hudcellerne, der differentierer til talgkirtler. Cellernes kerner farves blå; de lange strukturer er hårsække. Kredit:Universitetet i Turku Stamceller og -
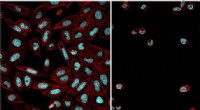 Lysfølsom trigger udviklet til den programmerede celledeling og dødCeller behandlet med den lysafhængige hæmmer (actincytoskelet i rødt, DNA i blåt) efter udsættelse for blåt lys (højre) og uden at aktivere blålysstråling (venstre). Kredit:Esther Zanin Ludwig Max
Lysfølsom trigger udviklet til den programmerede celledeling og dødCeller behandlet med den lysafhængige hæmmer (actincytoskelet i rødt, DNA i blåt) efter udsættelse for blåt lys (højre) og uden at aktivere blålysstråling (venstre). Kredit:Esther Zanin Ludwig Max -
 Chiton mollusk giver model til nyt panserdesignChiton bløddyr, som er omkring 1 til 2 tommer lang, har en serie på otte store plader og er omgivet af et bælte af mindre, mere fleksible vægte. Bløddyret er inspirationen bag en 3D-printet rustning.
Chiton mollusk giver model til nyt panserdesignChiton bløddyr, som er omkring 1 til 2 tommer lang, har en serie på otte store plader og er omgivet af et bælte af mindre, mere fleksible vægte. Bløddyret er inspirationen bag en 3D-printet rustning. -
 En hurtig, letanvendelig DNA-amplifikationsmetode ved 37 CelciusEn DNA-streng (lilla) primer eksponentiel amplifikation af DNA (rød) som signaler til at dirigere lysemission af DNA-nanodevices. Kredit:Organisk og biomolekylær kemi Forskere i Japan har udviklet
En hurtig, letanvendelig DNA-amplifikationsmetode ved 37 CelciusEn DNA-streng (lilla) primer eksponentiel amplifikation af DNA (rød) som signaler til at dirigere lysemission af DNA-nanodevices. Kredit:Organisk og biomolekylær kemi Forskere i Japan har udviklet
- Video:Skal du tisse på et vandmandsstik?
- Hvilke betingelser kræves for livet?
- Hvilke strukturer har bakterier XY?
- Hvorfor består enhver organisme af en eller flere celle?
- Nyt NIST-projekt til at bygge nano-termometre kan revolutionere temperaturbilleddannelse
- Hvad er den resulterende forskydning i en position, hvor destruktiv interferens er færdig?


