Hvad er forskellen mellem oxidation og hydrolyse?
Oxidation:
* Definition: Oxidation er tab af elektroner ved et molekyle, atom eller ion. Det kan også defineres som forstærkning af ilt eller tab af brint .
* Eksempler:
* Rusting: Jern (Fe) mister elektroner og kombineres med ilt for at danne jernoxid (Fe2O3), almindeligt kendt som rust.
* forbrænding: Brændstof (som træ) reagerer med ilt, frigiver energi og danner kuldioxid og vand.
* respiration: Glukose oxideres i vores celler og frigiver energi til vores kroppe.
Hydrolyse:
* Definition: Hydrolyse er nedbrydning af et molekyle ved tilsætning af vand . Det involverer spaltning af en kemisk binding ved tilsætning af et vandmolekyle.
* Eksempler:
* fordøjelse: Vores kroppe bruger hydrolyse til at nedbryde komplekse kulhydrater, proteiner og fedt i enklere molekyler, der kan absorberes.
* Sukkeropløsning: Sucrose (bordsukker) hydrolyseres i vand for at danne glukose og fruktose.
* sammenbrud af polymerer: Hydrolyse nedbryder polymerer som stivelse og cellulose i deres konstituerende monomerer.
Nøgleforskelle:
| Funktion | Oxidation | Hydrolyse |
| ---------------- | ----------------------------------------------------------------------------------------------------- |
| mekanisme | Tab af elektroner eller forstærkning af ilt/tab af brint | Spaltning ved vandtilsætning |
| resultat | Dannelse af nye forbindelser (er) med forskellige oxidationstilstande | Opdeling af et molekyle i mindre molekyler |
| Eksempler | Rusting, brændende, respiration | Fordøjelse, sukkeropløsning, polymernedbrydning |
Kortfattet:
* Oxidation involverer en ændring i antallet af elektroner i et molekyle.
* Hydrolyse involverer brud på et molekyle ved tilsætning af vand.
De er forskellige processer, selvom de kan forekomme samtidig i nogle reaktioner. For eksempel involverer oxidationen af glukose i cellulær respiration hydrolysereaktioner.
 Varme artikler
Varme artikler
-
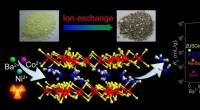 Selektiv indfangning af ioner fra spildevand med lagdelt metalsulfidSelektiv fangst af Ba 2 + , Ni 2 + , og Co 2 + af en robust lagdelt metalsulfid. Kredit:Prof. FENG Det er vigtigt at udvikle kemisk selektive rensemidler for ioner såsom Ba 2 + , N
Selektiv indfangning af ioner fra spildevand med lagdelt metalsulfidSelektiv fangst af Ba 2 + , Ni 2 + , og Co 2 + af en robust lagdelt metalsulfid. Kredit:Prof. FENG Det er vigtigt at udvikle kemisk selektive rensemidler for ioner såsom Ba 2 + , N -
 Forskere opfinder lim aktiveret af magnetfelt(Venstre til højre) NTU Assoc Prof Terry Steele, Prof Raju V. Ramanujan og Dr. Richa Chaudhary holder forskellige bløde og hårde materialer, der er bundet af deres nye magnethærdende lim, kredit:NTU S
Forskere opfinder lim aktiveret af magnetfelt(Venstre til højre) NTU Assoc Prof Terry Steele, Prof Raju V. Ramanujan og Dr. Richa Chaudhary holder forskellige bløde og hårde materialer, der er bundet af deres nye magnethærdende lim, kredit:NTU S -
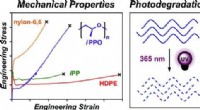 Kemikere skaber hurtigere nedbrydende plast til marinebrugKredit:ACS For at løse plastikmiljøkrisen, Cornell-kemikere har udviklet en ny polymer med rigelig styrke i marine omgivelser, der er klar til at nedbrydes af ultraviolet stråling, ifølge forsknin
Kemikere skaber hurtigere nedbrydende plast til marinebrugKredit:ACS For at løse plastikmiljøkrisen, Cornell-kemikere har udviklet en ny polymer med rigelig styrke i marine omgivelser, der er klar til at nedbrydes af ultraviolet stråling, ifølge forsknin -
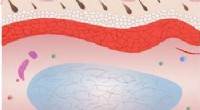 Hydrogel heler uden tilsætningsstofferEn illustration viser, hvordan over seks uger, fra top til bund, en hydrogel, der er udviklet ved Rice University, hjælper med vævsremodellering. Processen begynder med celleinfiltration efterfulgt af
Hydrogel heler uden tilsætningsstofferEn illustration viser, hvordan over seks uger, fra top til bund, en hydrogel, der er udviklet ved Rice University, hjælper med vævsremodellering. Processen begynder med celleinfiltration efterfulgt af
- 10 store spillere i den private sektors rumløb
- NOAA opgraderer den amerikanske globale vejrudsigtsmodel
- Hvad er enheden med størrelsesmagnetfelt?
- Vale beordrede at betale stammer 26,8 millioner dollars for forurening af floder
- Ny database sigter mod at accelerere udviklingen af elektrokatalysator gennem atom-skala indsigt
- Er den følgende sætning sand eller falsk sag undertiden kan omdannes til energi?


