Hvordan bruger et biologisk system brintbindinger?
1. Vand:
* højt kogepunkt og smeltepunkt: De stærke hydrogenbindinger mellem vandmolekyler giver det et relativt højt kogepunkt og smeltepunkt sammenlignet med andre molekyler af lignende størrelse. Dette gør det muligt for vand at forblive flydende over en lang række temperaturer, hvilket er vigtigt for livet.
* opløsningsmiddelegenskaber: Vandets evne til at danne brintbindinger gør det til et fremragende opløsningsmiddel for mange biologiske molekyler, herunder sukker, salte og proteiner. Dette muliggør transport og reaktion af disse molekyler i kroppen.
2. Proteiner:
* Sekundær struktur: Hydrogenbindinger mellem aminosyrer i polypeptidkæden er ansvarlige for dannelsen af alfa-helixer og beta-ark, to hovedelementer i protein sekundær struktur. Denne struktur er afgørende for proteinets samlede form og funktion.
* tertiær struktur: Hydrogenbindinger mellem aminosyresidekæder bidrager til dannelsen af proteinets tredimensionelle struktur, også kendt som tertiær struktur. Denne struktur definerer yderligere proteinets funktion og interaktioner med andre molekyler.
* kvartær struktur: Nogle proteiner består af flere polypeptidkæder (underenheder), der holdes sammen af brintbindinger, hvilket danner en kvartær struktur. Denne ordning er afgørende for proteinets aktivitet.
3. DNA og RNA:
* baseparring: Hydrogenbindinger holder de to DNA -tråde sammen og danner dobbelt helixstruktur. Disse bindinger forekommer mellem nitrogenholdige baser adenin (A) og thymin (T) og mellem guanin (G) og cytosin (C). Denne baseparring er vigtig for DNA -replikation og transkription.
* RNA -struktur: Hydrogenbindinger bidrager til foldning af RNA -molekyler til specifikke strukturer, som er essentielle for deres forskellige funktioner, herunder proteinsyntese og genregulering.
4. Carbohydrater:
* polysaccharidstruktur: Hydrogenbindinger spiller en rolle i at holde sammen de lange kæder af sukkermolekyler, der danner polysaccharider, såsom stivelse og cellulose. Denne struktur tilvejebringer vigtige strukturelle og energilagringsfunktioner i celler.
5. Cellemembraner:
* Membranfluiditet: Hydrogenbindinger mellem phospholipider, hovedkomponenten i cellemembraner, bidrager til membranens fluiditet, hvilket muliggør bevægelse af molekyler over membranen.
6. Enzymaktivitet:
* substratbinding: Hydrogenbindinger mellem enzymet og dets substrat kan hjælpe med at placere underlaget korrekt for katalyse, hvilket øger reaktionshastigheden.
7. Biologiske processer:
* Celleadhæsion: Hydrogenbindinger mellem celleoverflademolekyler hjælper celler med at klæbe til hinanden og danne væv og organer.
* Protein-proteininteraktioner: Hydrogenbindinger er vigtige for protein-proteininteraktioner, som er afgørende for mange biologiske processer, såsom signaltransduktion og regulering af genekspression.
Generelt er hydrogenbindinger en vigtig kraft i biologiske systemer, hvilket bidrager til en lang række vigtige funktioner, herunder struktur, funktion og stabilitet. De er nøglen til stabiliteten af makromolekyler, deres interaktion med andre molekyler og korrekt funktion af biologiske processer.
 Varme artikler
Varme artikler
-
 Levende celler integreret i fine strukturer skabt i en 3D-printerCeller, der breder sig i et 3D-stillads-fra venstre mod højre:uge 1, uge 3 uge 5. Top:3D-opsætning, bund:kun et lag. Kredit:Vienna University of Technology Vævsvækst og cellers adfærd kan kontroll
Levende celler integreret i fine strukturer skabt i en 3D-printerCeller, der breder sig i et 3D-stillads-fra venstre mod højre:uge 1, uge 3 uge 5. Top:3D-opsætning, bund:kun et lag. Kredit:Vienna University of Technology Vævsvækst og cellers adfærd kan kontroll -
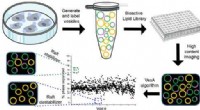 Biokemisk teknik til at finde små molekyler opdaget af forskereGrafisk abstrakt. Kredit:ACS Central Science (2022). DOI:10.1021/acscentsci.1c01058 Lipid-flåder, en komponent af plasmamembranerne, der omgiver alle celler i den menneskelige krop, er essentielle
Biokemisk teknik til at finde små molekyler opdaget af forskereGrafisk abstrakt. Kredit:ACS Central Science (2022). DOI:10.1021/acscentsci.1c01058 Lipid-flåder, en komponent af plasmamembranerne, der omgiver alle celler i den menneskelige krop, er essentielle -
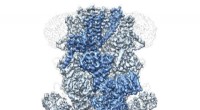 Cryo-EM afslører strukturen af protein, der er ansvarlig for at regulere kropstemperaturenCryo-EM billede af TRPM2. Kredit:Wei Lü og Juan Du Et team ledet af Van Andel Research Institute (VARI) forskere har for første gang afsløret strukturen på atomniveau for TRPM2, et protein, der ka
Cryo-EM afslører strukturen af protein, der er ansvarlig for at regulere kropstemperaturenCryo-EM billede af TRPM2. Kredit:Wei Lü og Juan Du Et team ledet af Van Andel Research Institute (VARI) forskere har for første gang afsløret strukturen på atomniveau for TRPM2, et protein, der ka -
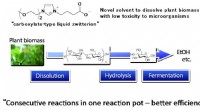 Nyt opløsningsmiddel bidrager til næste generations biobrændstofproduktion fra biomasseEfter opløsning af plantebiomasse med det nye opløsningsmiddel, flydende zwitterion af carboxylattypen, hydrolyse og fermentering blev udført fortløbende i en reaktionsbeholder til omdannelse til etha
Nyt opløsningsmiddel bidrager til næste generations biobrændstofproduktion fra biomasseEfter opløsning af plantebiomasse med det nye opløsningsmiddel, flydende zwitterion af carboxylattypen, hydrolyse og fermentering blev udført fortløbende i en reaktionsbeholder til omdannelse til etha
- Robotik, kodning bliver børns leg:KOOV Trial Kit
- Stærkere sort solbelægning, der bevarer originale farve og absorberende egenskaber
- Hvad var den måne Maria dannet fra?
- Hvilken grøn organelle findes kun i planter, og hvad er dens funktioner?
- Flyve hjem? Istiden kan have afskåret fugletræk
- Hvilke 2 hovedvæv udgør en plante rod?


